
6. 理解燃燒熱的概念,認識能源是人類生存和發展的重要基礎,了解化學在解決能源危機中的重要作用。知道節約能源、提高能量利用效率的實際意義。
5. 理解蓋斯定律的意義,能用蓋斯定律和熱化學方程式進行有關反應熱的簡單計算。
4. 認識熱化學方程式的意義并能正確書寫熱化學方程式。
3. 了解反應熱和焓變的涵義。
2. 認識化學反應過程中同時存在著物質和能量的變化,而且能量的釋放或吸收是以發生變化的物質為基礎的,能量的多少取決于反應物和生成物的質量。
1. 了解化學反應中能量轉化的原因和常見的能量轉化形式。
1、 為什么可燃物有氧氣參與,還必須達到著火點才能燃燒?
3、基本概念
1)什么是有效碰撞?
引起分子間的化學反應的碰撞是有效碰撞,分子間的碰撞是發生化學反應的必要條件,有效碰撞是發生化學反應的充分條件,某一化學反應的速率大小與,單位時間內有效碰撞的次數有關
2)什么是活化分子?
具有較高能量,能夠發生有效碰撞的分子是活化分子,發生有效碰撞的分子一定是活化分子,但活化分子的碰撞不一定是有效碰撞。有效碰撞次數的多少與單位體積內反應物中活化分子的多少有關。
3)什么是活化能?
活化分子高出反應物分子平均能量的部分是活化能,如圖
活化分子的多少與該反應的活化能的大小有關,
活化能的大小是由反應物分子的性質決定,(內因)活化能越小則一般分子成為活化分子越容易,則活化分子越多,則單位時間內有效碰撞越多,則反應速率越快。
4)什么是催化劑?催化劑是能改變化學反應的速率,但反應前后本身性質和質量都不改變的物質,催化劑作用:可以降低化學反應所需的活化能,也就等于提高了活化分子的百分數,從而提高了有效碰撞的頻率.反應速率大幅提高.
)歸納總結:一個反應要發生一般要經歷哪些過程?
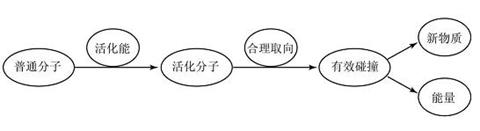
課堂思考題
2、化學反應原理所研究的范圍是
1)化學反應與能量的問題
2)化學反應的速率、方向及限度的問題
3)水溶液中的離子反應的問題
4)電化學的基礎知識
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com