

���һ��(g��)���W(xu��)����(y��ng)�У�����(y��ng)��Ŀ�������������Ŀ���������D��ʾ���P(gu��n)ϵ���tԓ����(y��ng)�^(gu��)���е�����׃����������(��şᡱ�����ᡱ)��
17.(12��)�����W(xu��)֪�R(sh��)ϵ�y(t��ng)���������ڌ�(du��)���W(xu��)��(w��n)�}���M(j��n)һ���J(r��n)�R(sh��)��Ո(q��ng)�ㅢ�c�����P(gu��n)�ڻ��W(xu��)����(y��ng)��ӑՓ��
��(w��n)�}1����ͬ���W(xu��)����(y��ng)�M(j��n)�еĿ����ͳ̶�ǧ���f(w��n)�e������(y��ng)�Ŀ����ͳ̶��ǻ������a(ch��n)���]�ăɂ�(g��)��Ҫ���ء�Ո(q��ng)�㰴�ձ���Ҫ������±�(���(n��i)�ݲ����؏�(f��))��
��̖(h��o)
��(sh��)�H���a(ch��n)�в�ȡ�Ĵ�ʩ
���I(y��)���a(ch��n)��(sh��)��(�����Q)
(1)
ͨ�^(gu��)����(qi��ng)���ԭ���D(zhu��n)����
(2)
ʹ�ô�������(y��ng)������
��(w��n)�}2�����W(xu��)����(y��ng)�İl(f��)�����Зl���ġ�����(y��ng)����ͬ������(y��ng)�ėl����ͬ������(y��ng)��ԭ����ͬ���磺4Na��O2===2Na2O��2Na��O2Na2O2 ����(sh��)��߀���S���l������Ӱ푻��W(xu��)����(y��ng)�İl(f��)����Ո(q��ng)���x�ӷ���(y��ng)����ʽ��ʾ�����^�c(di��n)������(y��ng)����ͬ������(y��ng)��ĝ�Ȳ�ͬ������(y��ng)��ԭ����ͬ����
��(w��n)�}3�����W(xu��)����(y��ng)�о����S��������׃����
16.ij�W(xu��)������100mL 1mol/L��������Һ���M(j��n)�����в�����Ȼ��(du��)��Һ��������_�y(c��)�����l(f��)�F(xi��n)�挍(sh��)���С��1mol/L���������в�����ʹ?ji��)��ƫ�͵��?��)
�� ����Ͳ��(l��i)��ȡ����ĝ�����r(sh��)��ҕ�x��(sh��)
�� ��Ͳ�Н�����ȫ���D(zhu��n)�Ƶ�������ϡጣ����D(zhu��n)�Ƶ�100mL����ƿ�У�����δϴ��
�� �ò�����������������Һ�D(zhu��n)�Ƶ�����ƿ�У�����Һ��������ƿ����
�� ���z�^�ιܼ����sˮ�r(sh��)��������μ��룬���ʹ��ҺҺ�泬�^(gu��)�˿̶Ⱦ����������õι���ȥ�����ˮ��ʹ��Һ�İ�Һ��ǡ���c�̶Ⱦ�����
A.�ڢۢ� B.�ۢ� C.�٢ڢ� D.�٢ڢۢ�
�}̖(h��o)
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
��
�ڢ��(���x���}����52��)
15.���Ќ�(sh��)�(y��n)�b�ÈD��ȫ���_����(��)
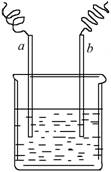
A.ԓ�b�ÿ�����늽��
B.a�O��һ���l(f��)��߀ԭ����(y��ng)
C.a��b������ͬ�N늘O����
D.ԓ�^(gu��)�����������D(zhu��n)�Qһ���ǻ��W(xu��)���D(zhu��n)�������
14.�҈D�У���늘O�ϰl(f��)����늘O����(y��ng)���£�a�O��Cu2����2e����Cu��b�O��
Fe��2e����Fe2�����t�����f(shu��)�������_����(��)
13.ij��Na���Ľ�������Һ�У�߀���ܺ�NH��Fe2����Br����CO��I����SO��6�N�x���еĎN���F(xi��n)�M(j��n)������(sh��)�(y��n)��
����ԭ��Һ�еμ�������ˮ���К��ݮa(ch��n)������Һ�ʳ��Sɫ��
����ʳ��Sɫ��Һ�м���BaCl2��Һ�r(sh��)�o(w��)�������ɣ�
�۳��Sɫ��Һ����ʹ����׃�{(l��n).
�ɴ��Ɣ�ԓ��Һ�϶����ڵ��x�Ӟ�(��)
A.Na����Fe3����SO��CO B.Na����NH��Fe2����CO
C.Na����Fe2����Br����I�� D.NH��Na����Br����CO
A.�ڢ�A�A����Ԫ���c��AԪ�����γɵĻ������ڹ̑B(t��i)�r(sh��)���x�Ӿ��w�����w��ꎡ��(y��ng)�x�����з�ʽ��ͬ
B.���w�д�����x�Ӿͱض������(y��ng)�x�ӣ������(y��ng)�x�Ӿͱض�������x��
C.�x�Ӿ��w��ֻ�����x���I�����Ӿ��w��ԭ�Ӿ��w�бض����й��r(ji��)�I
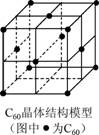
D.C60���w(��Y(ji��)��(g��u)ģ�����҈D)��ÿ��(g��)C60�����܇��c�����x����ҵȾ��x��C60������12��(g��)
�ٶ����� - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o(w��)���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com