
1.藥品的取用、加熱、
例4 根據以下敘述,回答1-2小題。1995年諾貝爾化學獎授予致力于研究臭氧層被破壞問題的三位環境化學家。大氣中的臭氧層可濾除大量的紫外光,保護地球上的生物。氟利昂(如CCl2F2)可在光的作用下分解,產生Cl原子,Cl原子會對臭氧層產生長久的破壞作用(臭氧的分子式為O3)。
有關反應為:
O3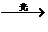 O2+O Cl+O3→ClO+O2 CIO+O→CI+O2
O2+O Cl+O3→ClO+O2 CIO+O→CI+O2
總反應:2O3→3O2
1.在上述臭氧變成氧氣的反應過程中,Cl是( )
A.反應物 B.生成物 C.中間產物 D.催化劑
2.O3和OZ是( )
A.同分異構體 B.同系物 C.氧的同素異形體 D.氧的同位素
[解析] 本題以環保問題為題材。信息內容起點較高,但落點卻很低,只考查了中學化學中的幾個基本概念:催化劑和同素異形體等。因而只要把這些概念搞清楚,便很快選出正確答案。
本題正確選項為1.D、2.C
*[例5] 1956年李政道和楊振寧提出在弱相互作用中宇宙不守恒,并由吳健雄用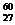 Co放射源進行了實驗驗證,次年,李、楊二人為此獲得諾貝爾物理獎,
Co放射源進行了實驗驗證,次年,李、楊二人為此獲得諾貝爾物理獎,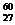 Co衰變過程是:
Co衰變過程是:
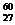 Co→
Co→ Ni+
Ni+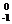 e+
e+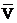 c
c
其中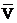 c 是反中微子,它的電荷為零,靜止質量可認為是零。
c 是反中微子,它的電荷為零,靜止質量可認為是零。
(1)Co與Fe同周期,它應在周期表的第____________周期,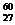 Co的核外電子數為____________,在上述衰變方程中,衰變產物
Co的核外電子數為____________,在上述衰變方程中,衰變產物 Ni的質量數A是____________,核電荷數Z是____________。
Ni的質量數A是____________,核電荷數Z是____________。
(2)在衰變前,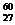 Co核靜止,根據云室照片可以看出,衰變產物
Co核靜止,根據云室照片可以看出,衰變產物 Ni和
Ni和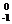 e的運動軌跡不在一條直線上,如果認為衰變產物只有Ni和
e的運動軌跡不在一條直線上,如果認為衰變產物只有Ni和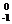 e,那么衰變過程將違背____________守恒定律。
e,那么衰變過程將違背____________守恒定律。
(3)無水CoCl2為深藍色,吸水后變為粉紅色的水合物,水合物受熱后又變成無水CoCl2,故常在實驗中用作吸濕劑和空氣濕度指示劑。
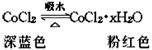
現有無水CoCl265g,吸水后變為CoCl2·xH2O119g,水合物中的x的值是____________。
(4)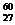 Co放出的γ射線,可用于作物誘變育種,我國應用該方法培育出了許多農作物新品種,如棉花高產品種“魯棉1號”,年種植面積達到3000多萬畝,在我國自己培育的棉花品種中栽培面積最大,γ射線處理作物后主要引起____________,從而產生可遺傳的變異,除γ射線外,用于人工誘變的其它理化因素還有____________、____________、____________和____________。
Co放出的γ射線,可用于作物誘變育種,我國應用該方法培育出了許多農作物新品種,如棉花高產品種“魯棉1號”,年種植面積達到3000多萬畝,在我國自己培育的棉花品種中栽培面積最大,γ射線處理作物后主要引起____________,從而產生可遺傳的變異,除γ射線外,用于人工誘變的其它理化因素還有____________、____________、____________和____________。
[解析]
本題以華裔科學家所獲諾貝爾獎成果為背景命題,試題介紹了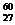 Co衰變方程,圍繞
Co衰變方程,圍繞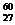 Co進行了多角度、多層次的設問,涉及到化學上的元素周期律、水合物,物理上的原子核結構、動量守恒定律,生物學上的人工誘變、基因變化等知識,考查學生運用理化生知識綜合分析事物的能力。第(1)問需要綜合物理、化學知識來解決,第(2)、(3)、(4)問分別用理化生知識解決,
Co進行了多角度、多層次的設問,涉及到化學上的元素周期律、水合物,物理上的原子核結構、動量守恒定律,生物學上的人工誘變、基因變化等知識,考查學生運用理化生知識綜合分析事物的能力。第(1)問需要綜合物理、化學知識來解決,第(2)、(3)、(4)問分別用理化生知識解決,
[答案] (1)4,27,28 (2)動量 (3)6 (4)基因突變,X射線、硫酸二乙酯、亞硝酸、紫外線、激光。
2.綠色化學:核心是利用化學原理從源頭上減少和消除工業生產對環境的影響。
原子利用率為期望產物的總質量與生成物的總質量之比。對于具體的化學反應,原子利用率等于期望生成物的摩爾質量與生成物的總摩爾質量之比。
原子利用率= 。
試題枚舉
例1石油煉制過程中,既能提高汽油產量又能提高汽油質量的方法 是( )
A 常壓分餾 B減壓分餾 C 裂解 D 催化裂化
[解析]選項中的四種方法都是石油煉制加工的方法,其目的不一樣,A項只能對石油進行初步加工,各類烴的質量僅占石油總量的25%左右。B項操作不會得到汽油,C項中所得產物主要是乙烯、丙烯等小分子短鏈化合物。只有D項能得到質量更高、產量更多的汽油。
答案: D
例2“綠色化學“要求從技術、經濟上設計出可行的化學反應,盡可能減少對環境的副作用。下列化學反應中,你認為最不符合綠色化學概念的是( )
A.除硫酸廠尾氣:SO2+2NH3+H2O=(NH4)2SO4
B.消除硝酸工業尾氣氮氧化物的污染:NO+NO2+2NaOH=2NaNO2+H2O
C.制硫酸銅:Cu+2H2SO4(濃) 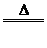 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
D.制硫酸銅:2Cu+O2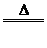 2CuO; CuO+H2SO4(稀)=CuSO4+H2O
2CuO; CuO+H2SO4(稀)=CuSO4+H2O
解析:A 、B的化學反應是對有害氣體的吸收,符合“綠色化學“的要求,C、D的目的是制硫酸銅,C中產生有毒的氣體SO2 ,會造成大氣污染,對比分析會發現D比C要節約原料,又不會產生有害氣體。
答案: C
例3工業上從海水中提取單質溴,其中有一種工藝采用如下方法:
(1) 向海水中通入氯氣將海水中的溴化物氧化,其離子方程式為:
(2) 向上述混合液中吹入熱空氣,將生成的溴吹出,用純堿溶液吸收,這時,溴就轉化成溴離子和溴酸根離子,其化學方程式為: 。
(3) 將(2)所得溶液用H2SO4酸化,又可得到單質溴,再用有機溶液萃取溴后,還可以得到副產品Na2SO4 。這一過程可用化學方程式表示為: 。
(4) 這樣得到的溴中還混有少量 Cl2,這樣除去Cl2 ?寫出反應的離子方程式:
。
解析:Cl2能將Br2從海水中置換出來,由于有:Br2+H2O=HBr+HBrO,大家往往會推測出Br2與純堿反應生成的鹽是NaBr和NaBrO。這樣推測是沒有注意審題,題中說Br2“轉化成溴離子和溴酸根離子”,所以生成的鹽是NaBr和NaBrO3。NaBr和NaBrO3的混合溶液用硫酸酸化,又可得到單質溴,顯然是發生了價態歸中的氧化還原反應。
答案:(1)Cl2+2Br-=Br2+2Cl-
(2)3Na2CO3+3Br2=5NaBr+NaBrO3+3CO2↑
(3)5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O
(4) Cl2+2Br-=Br2+2Cl-
1.環境污染:包括 , , 和食品污染。
2.海水化學資源的利用:(1)海鹽的生產:海水制鹽具有悠久的歷史,從海水中制取 , ,是在傳統海水制鹽工業上的發展。(2)Cl、Br、I的提取
1.海水水資源的利用:(1)海水的淡化:海水淡化的方法主要有 ,
。(2)直接利用海水進行循環冷卻。
天然氣既是一種清潔的能源,也是一種重要的化工原料,作為化工原料,它主要用于合成 和生產 。
2.煤的綜合利用:
 煤的干餾:把煤隔絕空氣加強熱使其分解的過程。得到焦炭、粗氨水、煤焦油、焦爐煤氣等
煤的干餾:把煤隔絕空氣加強熱使其分解的過程。得到焦炭、粗氨水、煤焦油、焦爐煤氣等
煤的氣化:把煤中的有機物轉化成可燃性氣體(CO、H2)的過程
煤的液化:把煤中的有機物轉化成可燃性液體(如CH3OH)的過程
1.煤的組成:主要含C元素。由有機物和無機物組成復雜的混合物。
2.石油的煉制
(1) 分餾:
原理:利用各組分沸點的不同將復雜混合物分離的過程。
方法:常壓分餾得到汽油、煤油、柴油、重油等產品。
減壓分餾
(2)石油的加工
裂化:一定條件下,使長鏈烴斷裂成短鏈烴的過程。目的是提高汽油的產量和質量
裂解:深度的裂化。目的是獲得短鏈的不飽和氣態烴。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com