
(1)受熱易分解,放出氨氣:NH4Cl
2)裝置特點:固+固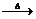 氣體,與制O2相同。
氣體,與制O2相同。
3)收集:向下排空氣法。
4)驗滿:a.
b.
5) 干燥:用堿石灰(NaOH與CaO的混合物)或生石灰在干燥管或U型管中干燥。不能用CaCl2、P2O5、濃硫酸作干燥劑,因為NH3能與CaCl2反應生成CaCl2?8NH3。P2O5、濃硫酸均能與NH3反應,生成相應的鹽。所以NH3通常用堿石灰干燥。
(4)氨氣的用途:液氨易揮發,汽化過程中會吸收熱量,使得周圍環境溫度降低,因此,液氨可以作制冷劑。
4、銨鹽
銨鹽均易溶于水,且都為白色晶體(很多化肥都是銨鹽)。
NH3?H2O NH3 ↑+H2O
NH3 ↑+H2O
氨水中的微粒: (六種微粒)。
噴泉實驗的原理:是利用氣體極易被一種液體吸收而形成壓強差,使容器內氣體壓強降低,外界大氣壓把液體壓入氣體容器內,在玻璃導管尖嘴處形成美麗的“噴泉”。
噴泉實驗成功的關鍵:(1)氣體在吸收液中被吸收得既快又多,如NH3、HCl、HBr、HI用水吸收,CO2、SO2,Cl2、H2S等用NaOH溶液吸收等。(2)裝置的氣密性要好。(3)燒瓶內的氣體純度要大。
b.氨氣可以與酸反應生成鹽:
①NH3+HCl=NH4Cl ②NH3+HNO3=NH4NO3 ③ 2NH3+H2SO4=(NH4)2SO4
因NH3溶于水呈堿性,所以可以用濕潤的紅色石蕊試紙檢驗氨氣的存在,因濃鹽酸有揮發性,所以也可以用蘸有濃鹽酸的玻璃棒靠近集氣瓶口,如果有大量白煙生成,可以證明有NH3存在。
(3)氨氣的實驗室制法:(課本P88圖4-33)
1)原理:
a.溶于水溶液呈 性:NH3+H2O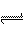 NH3?H2O
NH3?H2O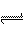 NH4++OH-
NH4++OH-
生成的一水合氨NH3?H2O是一種弱堿,很不穩定,受熱會分解:
3、氨氣(NH3)
(1)氨氣的物理性質:極易溶于水,有刺激性氣味,易液化。
(2)氨氣的化學性質:
常溫下,Fe、Al遇濃H2SO4或濃HNO3發生鈍化,(說成不反應是不妥的),加熱時能發生反應:Fe+6HNO3(濃) Fe(NO3)3+3NO2↑+3H2O
Fe(NO3)3+3NO2↑+3H2O
 (催化劑:粉塵、五氧化二釩)
(催化劑:粉塵、五氧化二釩)
(將SO2氣體和Cl2氣體混合后作用于有色溶液,漂白效果將大大減弱。)
④SO2的弱氧化性:如2H2S+SO2=3S↓+2H2O(有黃色沉淀生成)
⑤SO2的漂白性:SO2能使品紅溶液褪色,加熱會恢復原來的顏色。用此可以檢驗SO2的存在。
SO2
Cl2
漂白的物質
漂白某些有色物質
使濕潤有色物質褪色
原理
與有色物質化合生成不穩定的無色物質
與水生成HClO,HClO具有漂白性,將有色物質氧化成無色物質
加熱
能恢復原色(無色物質分解)
不能復原
⑥SO2的用途:漂白劑、殺菌消毒、生產硫酸等。
4、硫酸(H2SO4)
(1)濃硫酸的物理性質:純的硫酸為無色油狀粘稠液體,能與水以任意比互溶(稀釋濃硫酸要規范操作:注酸入水且不斷攪拌)。不揮發,沸點高,密度比水大。
(2)濃硫酸三大性質:
①吸水性:濃硫酸可吸收結晶水、濕存水和氣體中的水蒸氣,可作干燥劑,可干燥H2、
O2、SO2、CO2等氣體,但不可以用來干燥NH3、H2S氣體。
②脫水性:能將有機物(蔗糖、棉花等)以H和O原子個數比2┱1脫去,炭化變黑。
③強氧化性:濃硫酸在加熱條件下顯示強氧化性(+6價硫體現了強氧化性),能與大多數金屬反應,也能與非金屬反應。
(?)與大多數金屬反應(如銅):(此反應濃硫酸表現出酸性和強氧化性 )
(?)與非金屬反應(如C反應):(此反應濃硫酸表現出強氧化性 )
注意:常溫下,Fe、Al遇濃H2SO4或濃HNO3發生鈍化,而不是不反應。
濃硫酸的強氧化性使許多金屬能與它反應,但在常溫下,鋁和鐵遇濃硫酸時,因表面被濃硫酸氧化成一層致密氧化膜,這層氧化膜阻止了酸與內層金屬的進一步反應。這種現象叫金屬的鈍化。鋁和鐵也能被濃硝酸鈍化,所以,常溫下可以用鐵制或鋁制容器盛放濃硫酸和濃硝酸。
(3)、硫酸的用途:干燥劑、化肥、炸藥、蓄電池、農藥、醫藥等。
點評:SO2的性質及酸雨一直是高考命題的熱點內容,如SO2的漂白性,還原性等。特別注意:能使下列物質褪色體現的是SO2的何種性質?能使溴水、氯水、高錳酸鉀溶液褪色;能使酚酞試液變紅的溶液褪色等。將SO2通入BaCl2溶液中,是否有沉淀生成?若再通入足量的氨氣、氯氣是否產生白色沉淀?原理是什么?寫出對應的化學方程式。
氮及其化合物
1、氮的氧化物:NO2和NO
N2+O2 ======== 2NO,生成的一氧化氮很不穩定: 2NO+O2 == 2NO2
一氧化氮:無色氣體,有毒,能與人血液中的血紅蛋白結合而使人中毒(與CO中毒原理相同),難溶于水,是空氣中的污染物。
二氧化氮:紅棕色氣體(與溴蒸氣顏色相同)、有刺激性氣味、有毒、易液化、易溶于水,并與水反應:
3NO2+H2O=2HNO3+NO,此反應中NO2既是氧化劑又是還原劑。
以上三個反應是“雷雨固氮”、“雷雨發莊稼”的反應。
2、硝酸(HNO3):
(1)硝酸物理性質:純硝酸是無色、有刺激性氣味的油狀液體。低沸點(
(2)硝酸的化學性質:具有一般酸的通性,稀硝酸遇紫色石蕊試液變紅色,濃硝酸的氧化性比稀硝酸強。濃硝酸和稀硝酸都是強氧化劑,能氧化大多數金屬,但不放出氫氣,通常濃硝酸產生NO2,稀硝酸產生NO,如:
①Cu+4HNO3(濃)=
②3Cu+8HNO3(稀)=
反應①還原劑與氧化劑物質的量之比為 ;反應②還原劑與氧化劑物質的量之比為 。
漂白粉久置空氣會失效(涉及兩個反應):Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,  ↑,漂白粉變質會有CaCO3存在,外觀上會結塊,久置空氣中的漂白粉加入濃鹽酸會有CO2氣體生成,含CO2和HCl雜質氣體。
↑,漂白粉變質會有CaCO3存在,外觀上會結塊,久置空氣中的漂白粉加入濃鹽酸會有CO2氣體生成,含CO2和HCl雜質氣體。
⑤氯氣的用途:制漂白粉、自來水殺菌消毒、農藥和某些有機物的原料等。
2、Cl-的檢驗:
原理:根據Cl-與Ag+反應生成不溶于酸的AgCl沉淀來檢驗Cl-存在。
方法:先加硝酸化溶液(排除CO32-、SO32-干擾),再滴加AgNO3溶液,如有白色沉淀生成,則說明有Cl-存在。
點評:氯氣的強氧化性及氯水的漂白性是一直是高考的命題的熱點,如Cl2氧化Fe2+、Cl2氧化SO2等,另外,與生活聯系比較密切的漂白液、漂白粉及漂白精等內容,也較為重要。在2008年的高考實驗中,讓你根據制取氯氣的反應原理,選取合適的實驗裝置。
硫及其化合物
1、硫元素的存在:硫元素最外層電子數為6個,化學性質較活潑,容易得到2個電子呈-2價或者與其他非金屬元素結合成呈+4價、+6價化合物。硫元素在自然界中既有____態, 又有 態。(如火山口中的硫就以 存在)
2、硫單質:①物質性質:俗稱硫磺,淡黃色固體,不溶于水,熔點低。
②化學性質:S+O2 === SO2(空氣中點燃淡藍色火焰,純氧中為藍紫色)
3、二氧化硫(SO2)
(1)物理性質:易溶于水,有毒氣體,易液化。
(3)化學性質:
①SO2能與水反應:亞硫酸為中強酸,此反應為可逆反應。
可逆反應定義:在相同條件下,正逆方向同時進行的反應。(關鍵詞:相同條件下)
②SO2為酸性氧化物,可與堿反應生成鹽和水。
a、與NaOH溶液反應:SO2(少量)+2NaOH=Na2SO3+H2O
SO2(過量)+NaOH=NaHSO3
對比CO2與堿反應:CO2(少量)+Ca(OH)2=CaCO3↓(白色)+H2O
2CO2(過量)+Ca(OH)2=Ca(HCO3) 2 (可溶)
將SO2逐漸通入Ca(OH)2溶液中先有白色沉淀生成,后沉淀消失,與CO2逐漸通入Ca(OH)2溶液實驗現象相同,所以不能用石灰水來鑒別SO2和CO2。能使石灰水變渾濁的無色無味的氣體一定是二氧化碳,這說法是對的,因為SO2是有刺激性氣味的氣體。
b、SO2將通入酚酞變紅的溶液,溶液顏色褪去,體現了SO2和水反應生成亞硫酸,是酸性氧化物的性質,而不是漂白性,SO2不能漂白指示劑。
③SO2具有強還原性,能與強氧化劑(如酸性高錳酸鉀溶液、氯氣、氧氣等)反應。SO2能使酸性KMnO4溶液、新制氯水褪色,顯示了SO2的強還原性(不是SO2的漂白性)。
③高溫下與堿性氧化物反應:SiO2+CaO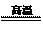 CaSiO3
CaSiO3
(4)用途:光導纖維、瑪瑙飾物、石英坩堝、石英鐘、儀器軸承、玻璃和建筑材料等。
(三)、硅酸(H2SiO3):
(1)物理性質:不溶于水的白色膠狀物,能形成硅膠,吸附水分能力強。
(2)化學性質:H2SiO3是一種弱酸,酸性比碳酸還要弱,但SiO2不溶于水,故不能直
接由SiO2溶于水制得,而用可溶性硅酸鹽與酸反應制取:(強酸制弱酸原理)
. (此方程式證明酸性:H2SiO3<H2CO3)
(3)用途:硅膠作干燥劑、催化劑的載體。
(四)、硅酸鹽
硅酸鹽:硅酸鹽是由硅、氧、金屬元素組成的化合物的總稱。硅酸鹽種類很多,大多數難溶于水,最常見的可溶性硅酸鹽是Na2SiO3,Na2SiO3的水溶液俗稱水玻璃,又稱泡花堿,是一種無色粘稠的液體,可以作黏膠劑和木材防火劑。硅酸鈉水溶液久置在空氣中容易變質:
. (有白色沉淀生成)
傳統硅酸鹽工業三大產品有:玻璃、陶瓷、水泥。
硅酸鹽由于組成比較復雜,常用氧化物的形式表示:活潑金屬氧化物→較活潑金屬氧化物→二氧化硅→水。
點評:有關硅及化合物知識,在高考中主要以選擇題的形式出現,考查硅及二氧化硅的用途,出現的頻率很高。
氯及其化合物
1、氯氣(Cl2):
(1)物理性質:黃綠色的有毒氣體,液氯為純凈物
(2)化學性質:氯氣化學性質非常活潑,很容易得到電子,作強氧化劑,能與金屬、非金屬、水以及堿反應。
①與金屬反應(將金屬氧化成最高正價)
Na+Cl2===2NaCl Cu+Cl2===CuCl2
2Fe+3Cl2===2FeCl3(氯氣與金屬鐵反應只生成FeCl3,而不生成FeCl2。)(鐵跟鹽酸反應生成FeCl2,而鐵跟氯氣反應生成FeCl3,這說明Cl2的氧化性強于鹽酸,是強氧化劑。)
②與非金屬反應
Cl2+H2 === 2HCl(氫氣在氯氣中燃燒現象:安靜燃燒,發出蒼白色火焰)
將H2和Cl2混合后在點燃或光照條件下發生爆炸。
③Cl2與水反應:離子方程式中,應注意次氯酸是弱酸,要寫成化學式而不能拆開。
將氯氣溶于水得到氯水(淺黃綠色),氯水含七種微粒,其中有 。
氯水的性質取決于其組成的微粒:
(1)強氧化性:Cl2是新制氯水的主要成分,實驗室常用氯水代替氯氣,如氯水中的氯氣能FeCl2反應。
(2)漂白、消毒性:氯水中的Cl2和HClO均有強氧化性,一般在應用其漂白和消毒時,
應考慮HClO,HClO的強氧化性將有色物質氧化成無色物質,不可逆。
(3)酸性:氯水中含有HCl和HClO,故可被NaOH中和,鹽酸還可與NaHCO3,CaCO3等反應。
(4)不穩定性:次氯酸見光易分解,久置氯水(淺黃綠色)會變成稀鹽酸(無色)失去漂白性。
(5)沉淀反應:加入AgNO3溶液有白色沉淀生成(氯水中有Cl-)。
自來水也用氯水殺菌消毒,所以用自來水配制以下溶液如FeCl2、Na2CO3、NaHCO3、AgNO3、NaOH等溶液會變質。
④Cl2與堿液反應:與NaOH反應:
與Ca(OH)2溶液反應:
此反應用來制漂白粉,漂白粉的主要成分為 ,有效成分為 。
漂白粉之所以具有漂白性,原因是:Ca(ClO)2+CO2+H2O==CaCO3↓+2HClO生成的HClO具有漂白性;同樣,氯水也具有漂白性,因為氯水含HClO;NaClO同樣具有漂白性,干燥的氯氣不能使紅紙褪色,因為不能生成HClO,濕的氯氣能使紅紙褪色,因為氯氣發生下列反應Cl2+H2O=HCl+HClO
2.用途:太陽能電池、計算機芯片以及良好的半導體材料等。
(二)、二氧化硅(SiO2):
(1)SiO2的空間結構:SiO2直接由原子構成,不存在單個SiO2分子。
(2)物理性質:熔點高,硬度大
(3)化學性質:SiO2常溫下化學性質很不活潑,不與水、酸反應(氫氟酸除外),能與強堿溶液、氫氟酸反應,高溫條件下可以與堿性氧化物反應:
①與強堿反應:生成的硅酸鈉
具有粘性,所以不能用帶磨口玻璃塞試劑瓶存放NaOH溶液和Na2SiO3溶液,避免Na2SiO3將瓶塞和試劑瓶粘住,打不開,應用橡皮塞)。
②與氫氟酸反應[SiO2的特性]:(利用此反應,氫氟酸能雕刻玻璃;氫氟酸不能用玻璃試劑瓶存放,應用塑料瓶)。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com