
44.



 (09年江蘇化學·18)(10分)二氧化氯(ClO2)是一種在水處理等方面有廣泛應用的高效安全消毒劑。與Cl2相比,ClO2不但具有更顯著地殺菌能力,而且不會產生對人體有潛在危害的有機氯代物。
(09年江蘇化學·18)(10分)二氧化氯(ClO2)是一種在水處理等方面有廣泛應用的高效安全消毒劑。與Cl2相比,ClO2不但具有更顯著地殺菌能力,而且不會產生對人體有潛在危害的有機氯代物。
 (1)在ClO2的制備方法中,有下列兩種制備方法:
(1)在ClO2的制備方法中,有下列兩種制備方法:
 方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
 方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O
 用方法二制備的ClO2更適合用于飲用水的消毒,其主要原因是
。
用方法二制備的ClO2更適合用于飲用水的消毒,其主要原因是
。
 (2)用ClO2處理過的飲用水(pH為5.5~6.5)常含有一定量對人體不利的亞氯酸根離子(ClO2-).2001年我國衛生部規定,飲用水ClO2-的含量應不超過0.2 mg·L-1。
(2)用ClO2處理過的飲用水(pH為5.5~6.5)常含有一定量對人體不利的亞氯酸根離子(ClO2-).2001年我國衛生部規定,飲用水ClO2-的含量應不超過0.2 mg·L-1。
 飲用水中ClO2、ClO2-的含量可用連續碘量法進行測定。ClO2被I-還原為ClO2-、Cl-的轉化率與溶液pH的關系如右圖所示。當pH≤2.0時,ClO2-也能被I-
飲用水中ClO2、ClO2-的含量可用連續碘量法進行測定。ClO2被I-還原為ClO2-、Cl-的轉化率與溶液pH的關系如右圖所示。當pH≤2.0時,ClO2-也能被I-

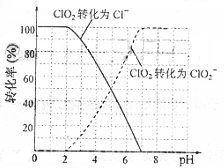 完全還原成Cl-。反應生成的I2用標準Na2S2O3溶液滴定:2Na2S2O3+I2=Na2S4O6+2NaI
完全還原成Cl-。反應生成的I2用標準Na2S2O3溶液滴定:2Na2S2O3+I2=Na2S4O6+2NaI
 ① 請寫出pH≤2.0時,ClO2-與I-反應的離子方程式
。
① 請寫出pH≤2.0時,ClO2-與I-反應的離子方程式
。
 ②請完成相應的實驗步驟:
②請完成相應的實驗步驟:
 步驟1:準確量取VmL水樣加入到錐形瓶中。
步驟1:準確量取VmL水樣加入到錐形瓶中。
 步驟2:調節水樣的pH為7.0~8.0
步驟2:調節水樣的pH為7.0~8.0
 步驟3:加入足量的KI晶體。
步驟3:加入足量的KI晶體。
 步驟4:加少量淀粉溶液,用c mol·L-1Na2S2O3溶液滴定至終點,消耗Na2S2O3溶液V1mL。
步驟4:加少量淀粉溶液,用c mol·L-1Na2S2O3溶液滴定至終點,消耗Na2S2O3溶液V1mL。
 步驟5: 。
步驟5: 。
 步驟6;再用c mol·L-1Na2S2O3溶液滴定至終點,消耗Na2S2O3溶液V2mL。
步驟6;再用c mol·L-1Na2S2O3溶液滴定至終點,消耗Na2S2O3溶液V2mL。
 ③根據上述分析數據,測得該引用水樣中的ClO2-的濃度為 mg·L-1(用含字母的代數式表示)。
③根據上述分析數據,測得該引用水樣中的ClO2-的濃度為 mg·L-1(用含字母的代數式表示)。
 ④若飲用水中ClO2-的含量超標,可向其中加入適量的,該反應的氧化產物是 (填化學式)
④若飲用水中ClO2-的含量超標,可向其中加入適量的,該反應的氧化產物是 (填化學式)
 答案:
答案:
(1)方法二制備的ClO2中不含Cl2
 (2)①ClO2-+4H++4I-=Cl-+2I2+2H2O
(2)①ClO2-+4H++4I-=Cl-+2I2+2H2O
 ②調節溶液的pH≤2.0
②調節溶液的pH≤2.0
 ③
③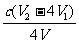
 ④Fe(OH)3
④Fe(OH)3

 解析:(1)比較簡單,觀察兩組方程式,看看產物結合其性質即能得出答案。(2)pH≤2.0時,ClO2-也能被I-
解析:(1)比較簡單,觀察兩組方程式,看看產物結合其性質即能得出答案。(2)pH≤2.0時,ClO2-也能被I- 完全還原成Cl-,那么I-要被氧化為碘單質,溶液是酸性溶液即可正確寫出離子方程式。題目信息提示用的是連續碘量法進行測定,步驟6又用Na2S2O3溶液滴定至終點,說明步驟5中有碘生成,結合① 請寫出pH≤2.0時,ClO2-與I-反應的離子方程式與pH為7.0~8.0的溶液中存在ClO-可以判斷調節溶液的pH≤2.0
完全還原成Cl-,那么I-要被氧化為碘單質,溶液是酸性溶液即可正確寫出離子方程式。題目信息提示用的是連續碘量法進行測定,步驟6又用Na2S2O3溶液滴定至終點,說明步驟5中有碘生成,結合① 請寫出pH≤2.0時,ClO2-與I-反應的離子方程式與pH為7.0~8.0的溶液中存在ClO-可以判斷調節溶液的pH≤2.0 。求引用水樣中的ClO2-的濃度可以用關系式法以碘單質為橋梁正確的找準ClO2-與Na2S2O3的關系。Fe2+將ClO2-還原成Cl-,Fe2+被氧化為鐵離子,結合反應物不難得出答案
。求引用水樣中的ClO2-的濃度可以用關系式法以碘單質為橋梁正確的找準ClO2-與Na2S2O3的關系。Fe2+將ClO2-還原成Cl-,Fe2+被氧化為鐵離子,結合反應物不難得出答案

 [考點分析]關注題目給與的信息從題目中挖掘有用的信息,注意關鍵詞如本題的連續碘量法。
[考點分析]關注題目給與的信息從題目中挖掘有用的信息,注意關鍵詞如本題的連續碘量法。
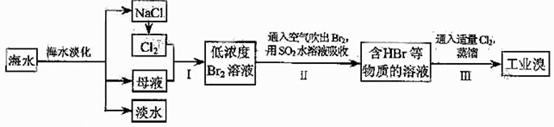
45 .(09年天津理綜·9)(18分)海水是巨大的資源寶庫,在海水淡化及綜合利用方面,天津市位居全國前列。從海水中提取食鹽和溴的過程如下:
.(09年天津理綜·9)(18分)海水是巨大的資源寶庫,在海水淡化及綜合利用方面,天津市位居全國前列。從海水中提取食鹽和溴的過程如下:

 (1)請列舉海水淡化的兩種方法: 、 。
(1)請列舉海水淡化的兩種方法: 、 。
 (2)將NaCl溶液進行電解,在電解槽中可直接得到的產品有H2、 、 、或H2、 。
(2)將NaCl溶液進行電解,在電解槽中可直接得到的產品有H2、 、 、或H2、 。
 (3)步驟Ⅰ中已獲得Br2,步驟Ⅱ中又將Br2還原為Br,其目的為
。
(3)步驟Ⅰ中已獲得Br2,步驟Ⅱ中又將Br2還原為Br,其目的為
。
 (4)步驟Ⅱ用SO2水溶液吸收Br2,吸收率可達95%,有關反應的離子方程式為 ,由此反應可知,除環境保護外,在工業生產中應解決的主要問題是
。
(4)步驟Ⅱ用SO2水溶液吸收Br2,吸收率可達95%,有關反應的離子方程式為 ,由此反應可知,除環境保護外,在工業生產中應解決的主要問題是
。
 (5)某化學研究性學習小組為了解從工業溴中提純溴的方法,查閱了有關資料,Br2的沸點為59℃。微溶于水,有毒性和強腐蝕性。他們參觀生產過程后,了如下裝置簡圖:
(5)某化學研究性學習小組為了解從工業溴中提純溴的方法,查閱了有關資料,Br2的沸點為59℃。微溶于水,有毒性和強腐蝕性。他們參觀生產過程后,了如下裝置簡圖:

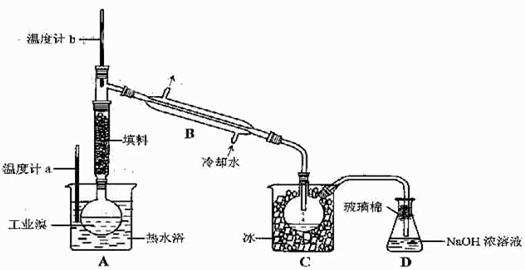
 請你參與分析討論:
請你參與分析討論:
 ①圖中儀器B的名稱:
。
①圖中儀器B的名稱:
。
 ②整套實驗裝置中儀器連接均不能用橡膠塞和橡膠管,其原因是
。
②整套實驗裝置中儀器連接均不能用橡膠塞和橡膠管,其原因是
。
 ③實驗裝置氣密性良好,要達到提純溴的目的,操作中如何控制關鍵條件:
。
③實驗裝置氣密性良好,要達到提純溴的目的,操作中如何控制關鍵條件:
。
 ④C中液體產生顏色為 。為除去該產物中仍殘留的少量Cl2,可向其中加入NaBr溶液,充分反應后,再進行的分離操作是
。
④C中液體產生顏色為 。為除去該產物中仍殘留的少量Cl2,可向其中加入NaBr溶液,充分反應后,再進行的分離操作是
。
答案:(1)蒸餾法、電滲析法、離子交換法及其其他合理答案中的任意兩種
(2)Cl2 NaOH NaClO
(3)富集溴元素
(4)Br2+SO2+2H2O=4H++SO42-+2Br- 強酸對設備的嚴重腐蝕
(5)①冷凝管 ②Br2腐蝕橡膠③控制溫度計b的溫度,并收集59℃的餾分④深紅棕色 分液(或蒸餾)
解析:本題考查海水中提取溴的實驗。電解NaCl溶液的方程式為:2NaCl
+ 2H2O 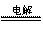 2NaOH+H2↑+Cl2↑,其中Cl2有可能與NaOH會生成NaClO。步驟I中的Br2的濃度很小,多次用SO2反復吸收,最終用Cl2處理,則可獲得大量的工業溴。溴具有強氧化性可以氧化SO2,生成H2SO4,因此要注意酸對設備的腐蝕問題。溴具有腐蝕性,可以腐蝕橡膠。蒸餾的目的,就是通過沸點不同而提純Br2,所以要通過溫度計控制好Br2沸騰的溫度,盡可能使Br2純凈。
2NaOH+H2↑+Cl2↑,其中Cl2有可能與NaOH會生成NaClO。步驟I中的Br2的濃度很小,多次用SO2反復吸收,最終用Cl2處理,則可獲得大量的工業溴。溴具有強氧化性可以氧化SO2,生成H2SO4,因此要注意酸對設備的腐蝕問題。溴具有腐蝕性,可以腐蝕橡膠。蒸餾的目的,就是通過沸點不同而提純Br2,所以要通過溫度計控制好Br2沸騰的溫度,盡可能使Br2純凈。
43. (09年海南化學·20.4)(11分)
(09年海南化學·20.4)(11分)
 工業上常用氨氧化法生產硝酸,其過程包括氨的催化氧化(催化劑為鉑銠合金絲網)、一氧化氮的氧化和水吸收二氧化氮生成硝酸。請回答下列問題:
工業上常用氨氧化法生產硝酸,其過程包括氨的催化氧化(催化劑為鉑銠合金絲網)、一氧化氮的氧化和水吸收二氧化氮生成硝酸。請回答下列問題:
 (1)氨催化氧化的化學方程式為
:
(1)氨催化氧化的化學方程式為
:
 (2)原料氣中空氣必須過量,其主要原因是
;
(2)原料氣中空氣必須過量,其主要原因是
;
 (3)將鉑銠合金做成薄絲網的主要原因是
;
(3)將鉑銠合金做成薄絲網的主要原因是
;
 (4)水吸收二氧化氮生成硝酸為放熱反應,其化學方程式為
,為了提高水對二氧化氮的吸收率,可采取的措施為
(答2項)。
(4)水吸收二氧化氮生成硝酸為放熱反應,其化學方程式為
,為了提高水對二氧化氮的吸收率,可采取的措施為
(答2項)。
答案:(11分)
(1)4NH3+5O2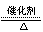 4NO+6H2O
4NO+6H2O (3分)
(3分)
 (2)提高氨的轉化率和一氧化氮的轉化率(2分)
(2)提高氨的轉化率和一氧化氮的轉化率(2分)
 (3)增大單位質量的催化劑與反應物的接觸面積(2分)
(3)增大單位質量的催化劑與反應物的接觸面積(2分)
 (4)3NO2+H2O=2HNO3+NO 加壓 降溫(4分)
(4)3NO2+H2O=2HNO3+NO 加壓 降溫(4分)
解析:(1)
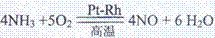
(2)根據平衡原理,增大反應物的濃度,平衡向正反應方向移動,以提高原料的轉化率;
(3)這是為了增大鉑銠合金的表面積,使接觸面積增大,提升催化的效果;
(4)為了提高吸收率,可根據溶解過程放熱采用降溫處理,且氣體的吸收可用加壓的方式。
42. (09年海南化學·16)(9分)
(09年海南化學·16)(9分)
 下圖表示從固體混合物中分離X的2種方案,請回答有關問題。
下圖表示從固體混合物中分離X的2種方案,請回答有關問題。

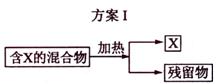

 (1)選用方案I時,X應該具有的性質是
,殘留物應該具有的性質是
;
(1)選用方案I時,X應該具有的性質是
,殘留物應該具有的性質是
;
 (2)選用方案Ⅱ從某金屬粉末(含有Au、Ag和Cu)中分離Au,加入的試劑是 ,有關反應的化學方程式為
;
(2)選用方案Ⅱ從某金屬粉末(含有Au、Ag和Cu)中分離Au,加入的試劑是 ,有關反應的化學方程式為
;
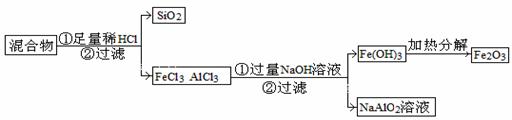
 (3)為提純某Fe2O3樣品(主要雜質有SiO2、A12O3),參照方案I和Ⅱ,請設計一種以框圖形式表示的實驗方案(注明物質和操作)
。
(3)為提純某Fe2O3樣品(主要雜質有SiO2、A12O3),參照方案I和Ⅱ,請設計一種以框圖形式表示的實驗方案(注明物質和操作)
。
答案:(9分)
 (1)有揮發性(或易升華)
受熱不揮發,且具有較高的熱穩定性(2分)
(1)有揮發性(或易升華)
受熱不揮發,且具有較高的熱穩定性(2分)
 (2)HNO3 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(2)HNO3 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
3Ag+4HNO3(稀)=3AgNO3+NO↑+2H2O
[或Cu+4HNO3(濃)=Cu(NO3)2+2NO2↑+2H2O
Ag+2HNO3(濃)=AgNO3+NO2↑+2H2O]

 (3分)
(3分)
 (3)
(3)
 (4分)(其他合理答案:也可給分)
(4分)(其他合理答案:也可給分)
解析:(1)從題中給的信息可理解為升華或蒸餾,因此X的性質為加熱時可升華,或易揮發。殘留物必須熱穩定性好,且沒有揮發性。
(2)金、銀、銅三種金屬金的活潑性最差,不能與硝酸反應,選用硝酸作為試劑,過濾即可。
(3)三種氧化物中,SiO2、Al2O3都能與強堿發生反應,但Fe2O3不會反應,可以選濃NaOH溶液反應后過濾。但如果SiO2的含量大,則不宜用前面所述方法,可選用鹽酸溶解,過濾后去除SiO2,再在混合液中加入過量的溶液,過濾得Fe(OH)3沉淀,洗滌后加熱分解的方法。
41. (09年海南化學·13)(9分)
(09年海南化學·13)(9分)
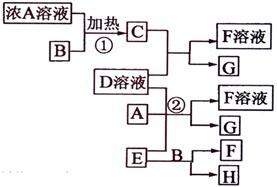
 有關物質存在如圖所示的轉化關系(部分產物已省略)。通常C為氣體單質,G為紫黑色固體單質。實驗室中,常用固體E在B的催化下加熱制取氣體單質H。
有關物質存在如圖所示的轉化關系(部分產物已省略)。通常C為氣體單質,G為紫黑色固體單質。實驗室中,常用固體E在B的催化下加熱制取氣體單質H。


 請回答下列問題:
請回答下列問題:
 (1)反應①的化學方程式為
(1)反應①的化學方程式為
 (2)反應②的離子方程式為
(2)反應②的離子方程式為
 (3)寫出另外一種實驗室制取H的化學方程式
(3)寫出另外一種實驗室制取H的化學方程式
 (4)D溶液與Pb(NO3)2溶液混合可形成沉淀,此沉淀的Ksp=7.0×10-9。將等體積的D溶液與Pb(NO3)2溶液混合,若D的濃度為1×10-2mo1/L
,則生成沉淀所需Pb(NO3)2溶液的最小濃度為
。
(4)D溶液與Pb(NO3)2溶液混合可形成沉淀,此沉淀的Ksp=7.0×10-9。將等體積的D溶液與Pb(NO3)2溶液混合,若D的濃度為1×10-2mo1/L
,則生成沉淀所需Pb(NO3)2溶液的最小濃度為
。
答案:(9分)


 (1)MnO2+4HCl(濃)
(1)MnO2+4HCl(濃) MnCl2+Cl2↑+2H2O(2分)
MnCl2+Cl2↑+2H2O(2分)
 (2)6I-+ClO3-+6H+=3I2+Cl-+3H2O(2分)
(2)6I-+ClO3-+6H+=3I2+Cl-+3H2O(2分)
 (3)2H2O2
(3)2H2O2 2H2O+O2↑或2KMnO4
2H2O+O2↑或2KMnO4 K2MnO4+MnO2+O2↑(其他合理答案:也給分)(2分)
K2MnO4+MnO2+O2↑(其他合理答案:也給分)(2分)
 (4)5.6×10-4mol·L-1(3分)
(4)5.6×10-4mol·L-1(3分)
解析:首先得破框圖,G為紫黑色固體單質,一般可預測為碘單質,可推得C物質為氯氣,則A為鹽酸、B為二氧化錳;E在二氧化錳的催化下制取H,則E為氯酸鉀、H為氧氣;F為氯化鉀;于是D一定為碘化鉀。所以推出A鹽酸、B二氧化錳、C氯氣、D碘化鉀、E氯酸鉀、F氯化鉀、G碘、H氧氣。
40.(16分)(08年山東理綜·30)食鹽是日常生活的必需品,也是重要的化工原料。
(1)粗食鹽常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等雜質離子,實驗室提純NaCl的流程如下:
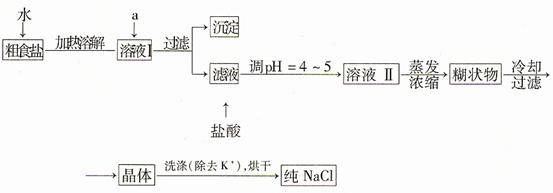
提供的試劑:飽和Na2CO3溶液 飽和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液 75%乙醇 四氯化碳
①欲除去溶液I中的+Ca2+、Mg2+、Fe3+、SO42-離子,選出a所代表的試劑,按滴加順序依次是 (只填化學式)。
②洗滌除去NaCl晶體表面附帶的少量KCl,選用的試劑為 。
(2)用提純的NaCl配制500 mL 4.00 mol·L-1 NaCl溶液,所用儀器除藥匙、玻璃棒外還有 (填儀器名稱)。
(3)電解飽和食鹽水的裝置如圖所示,若收集的H2為2 L,則同樣條件下收集的Cl2
 (填“>”、“=”或“<”)2 L,原因是
。裝置改進后可用于制備NaOH溶液,若測定溶液中NaOH的濃度,常用的方法為
。
(填“>”、“=”或“<”)2 L,原因是
。裝置改進后可用于制備NaOH溶液,若測定溶液中NaOH的濃度,常用的方法為
。
(4)實驗室制備H2和Cl2通常采用下列反應:
Zn+H2SO4=ZnSO4+H2↑
MnO2+4HCl(濃) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
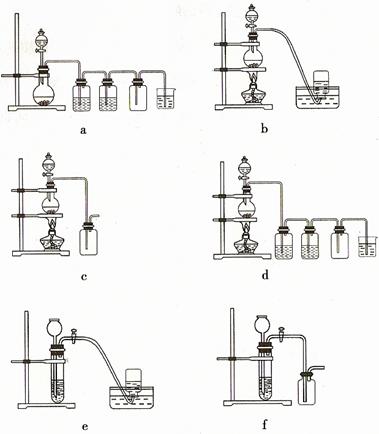
據此,從下列所給儀器裝置中選擇制備并收集H2的裝置 (填代號)和制備并收集干燥、純凈Cl2的裝置 (填代號)。
可選用制備氣體的裝置:
答案:
(1)①BaCl2、NaOH、Na2CO3(錯選或多選本小題不得分。NaOH溶液的加入順序及是否答Na0H不影響得分)
②75%乙醇
(2)天平、燒杯、500 mL容量瓶、膠頭滴管
(3)< 電解生成的氯氣與電解生成的NaOH發生了反應 酸堿中和滴定
(4)c d
解析:(1)①要除去SO42-,只有選BaCl2溶液,若選用Ba(NO3)2,會引入新的離子NO3-,再選用NaOH溶液除去Mg2+和Fe3+溶液,最后選用Na2CO3溶液除去Ca2+,此處不能選用K2CO3溶液,否則會引入新的K+,再用HCl除去過量的CO32-。Na2CO3溶液不能加在BaCl2溶液前,否則會引入Ba2+。②除去NaCl晶體表面的少量的KCl,應選用75%的乙醇,因為CCl4有毒,同時KCl也不會溶解在CCl4中。
(3)2NaCl+2H2O 2NaOH+Cl2↑+H2↑,在陰級區內產生的Cl2能與該區生成的NaOH反應NaCl、NaClO和H2O,使得部分的Cl2被消耗,所以同樣條件下收集到的Cl2小于2L。
2NaOH+Cl2↑+H2↑,在陰級區內產生的Cl2能與該區生成的NaOH反應NaCl、NaClO和H2O,使得部分的Cl2被消耗,所以同樣條件下收集到的Cl2小于2L。
39.(8分)(08年海南化學·13)下圖表示某固態單質A及其化合物之間的轉化關系(某些產物和反應條件已略去)。化合物B在常溫常壓下為氣體,B和C的相對分子質量之比為4︰5,化合物D是重要的工業原料。
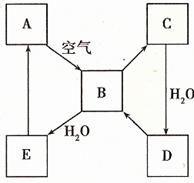
(1)寫出A在加熱條件下與H2反應的化學方程式___________________________。
(2)寫出E與A的氫化物反應生成A的化學方程式___________________________。
(3)寫出一個由D生成B的化學方程式____________________________________。
(4)將5 mL0.10 mol·L-1的E溶液與10 mL0.10 mol·L-1的NaOH溶液混合。
①寫出反應的離子方程式__________________________________________;
②反應后溶液的pH ____7(填“大于”、“小于”或“等于”),理由是 ;
③加熱反應后的溶液,其pH_____(填“增大”、“不變”或“減小”),理由是_______________。
答案:(8分)(1)H2+S H2S(寫成可逆反應也正確)
H2S(寫成可逆反應也正確)
(2)H2SO3 + 2H2S=3S + 3H2O
(3)C+2H2SO4(濃) CO2
↑+2SO2 ↑+2H2O(其他合理答案也給分如Cu+ 2H2SO4(濃)
CO2
↑+2SO2 ↑+2H2O(其他合理答案也給分如Cu+ 2H2SO4(濃) CuSO4
+SO2↑+ 2H2O等)
CuSO4
+SO2↑+ 2H2O等)
(4)①H2SO3 +2OH- = SO32- + 2H2O
②大于 Na2SO3溶液中SO32-發生水解使溶液顯堿性
③增大 升高溫度促進Na2SO3溶液的水解
解析:固態單質A能與空氣中的氧氣反應生成氣體物質B,則A可能為C或S等,假定為S,則B為SO2,C為SO3,它們的相對分子質量為64∶80=4∶5,恰好與題意相符(同時也證明A不是C),則D為H2SO4,它是一種重要的工業原料,與題意也相符,進一步證明A為S。E為H2SO3。
38.(11分)(08年廣東化學·23)
硅單質及其化合物應用范圍很廣。請回答下列問題:
(1)制備硅半導體材料必須先得到高純硅。三氯甲硅烷(SiHCl3)還原法是當前制備高純硅的主要方法,生產過程示意圖如下:

①寫出由純SiHCl3制備高純硅的化學反應方程式 。
②整個制備過程必須嚴格控制無水無氧。SiHCl3遇水劇烈反應生成H2SiO3、HCl和另一種物質,寫出配平的化學反應方程式 ;H2還原SiHCl3過程中若混O2,可能引起的后果是 。
(2)下列有頭硅材料的說法正確的是 (填字母)。
A.碳化硅化學性質穩定,可用于生產耐高溫水泥
B.氮化硅硬度大、熔點高,可用于制作高溫陶瓷和軸承
C.高純度的二氧化硅可用于制造高性能通訊材料--光導纖維
D.普通玻璃是由純堿、石灰石和石英砂制成的,其熔點很高
E.鹽酸可以與硅反應,故采用鹽酸為拋光液拋光單晶硅
(3)硅酸鈉水溶液俗稱水玻璃。取少量硅酸鈉溶液于試管中,逐滴加入飽和氯化銨溶液,振蕩。寫出實驗現象并給予解釋 。
答案:
(1)①SiHCl3+H2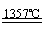
 Si+3HCl
Si+3HCl
②3SiHCl3+3H2O===H2SiO3↓+H2↑+3HCl 高溫下,H2遇O2發生爆炸
(2)BC
(3)生成白色絮狀沉淀,又刺激性氣味的氣體生成;解釋:SiO32-與NH4+發生雙水解反應,SiO32- + 2 NH4+ + 2H2O ===2NH3·H2O + H2SiO3↓
解析:(1) ①寫出由純SiHCl3制備高純硅的化學反應方程式:
SiHCl3+H2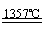
 Si+3HCl
Si+3HCl
②SiHCl3遇水劇烈反應生成H2SiO3、HCl和另一種物質,寫出配平的化學反應方程式3SiHCl3+3H2O====H2SiO3+H2↑+3HCl;H2還原SiHCl3過程中若混入O2,可能引起的后果是:高溫下,H2遇O2發生爆炸。
(2)ABCD
解釋:SiC和Si3N4均為原子晶體,熔點高,性質穩定,AB正確。光導纖維的材料為SiO2,C正確。普通玻璃的主要成分為Na2SiO3和CaSiO3,它是以石英砂(SiO2)、石灰石(CaCO3)和純堿(Na2CO3)為主要原料反應制成的。Na2CO3+SiO2 Na2SiO3+CO2;CaCO3+SiO2
Na2SiO3+CO2;CaCO3+SiO2 aSiO3+CO2,D正確。常溫下,Si只能與唯一一種酸HF反應不與HCl反應,E錯。
aSiO3+CO2,D正確。常溫下,Si只能與唯一一種酸HF反應不與HCl反應,E錯。
(3)寫出實驗現象并給予解釋:生成白色絮狀沉淀,又刺激性氣味的氣體生成;SiO32-與NH4+發生雙水解反應,SiO32- + 2 NH4+ + 2H2O ==== 2NH3·H2O + H2SiO3↓。
37.(07年山東理綜·30)(16分)下圖所示為常見氣體制備、分離、干爆和性質驗證的部分儀器裝置(加熱設備及夾持固定裝置均略去),請根據要求完成下列各題(儀器裝置可任意選用,必要時可重復選擇,a、b為活塞)。
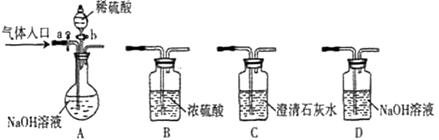
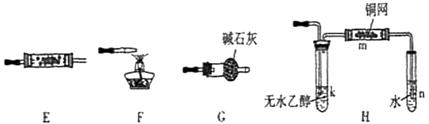
(1)若氣體入口通入CO和CO2的混合氣體,E內放置CuO,選擇裝置獲得純凈干燥的CO,并驗證其還原性及氧化產物,所選裝置的連接順序為 (填代號)。能驗證CO氧化產物的現象是 。
(2)停止CO和CO2混合氣體的通入,E內放置Na2O2,按A→E→D→B→H裝置順序制取純凈干燥的O2,并用O2氧化乙醇。此時,活塞a應 ,活塞b應 。需要加熱的儀器裝置有 (填代號),m中反應的化學方程式為 。
(3)若氣體入口改通空氣,分液漏斗內改改加濃氨水,圓地燒瓶內改加 NaOH 固體,E內裝有鉑鐒合金網,按A→G→E→D裝置程序制取干燥氧氣,并驗證氨的某些性質。
①裝置A中能產生氨氣的原因有: 。
②實驗中觀察到E內有紅棕色氣體現出,證明氨氣具有 性。
答案:(1)ACBECF AB之間的C裝置中溶液保持澄清,EF之同的C裝置中溶液變渾濁
(2)關閉 打開 k
m 2CH3CH2OH+O2 2CH3CHO+2H2O
2CH3CHO+2H2O
(3)①氫氧化鈉溶于水放出大量熱,溫度升高,使氨的溶解度減小而放出;氧氧化鈉吸水,促使氨放出;氫氧化鈉電離出的OH-增大了氨水中OH-濃度,促使氨水電離平衡左移,導致氨氣放出。②還原
解析:(1)根據實驗要求,A裝置中通入的氣體為CO和CO2的混合氣,在A中,CO2 被氫氧化鈉吸收,若要獲得純凈干燥的CO,需要選取裝置C,證明CO2 被除盡,然后通過盛有濃硫酸的B除去水蒸氣,要驗證CO的還原性,需要裝有CuO的裝置E,驗證CO的氧化產物CO2 ,還需要裝置C,最后需要F除去為反應的CO。所選裝置的連接順序是ACBECF,能驗證CO的氧化產物的實驗現象是:AB之間的C裝置中溶液保持澄清,EF之間的C裝置中溶液變渾濁。
(2)停止通入CO和CO2
的混合氣體,需要關閉活塞a,然后打開活塞b,此時稀硫酸與碳酸鈉溶液(CO2
與NaOH反應生成的)反應,反應生成的CO2氣體進入E中,并與 與Na2O2反應產生氧氣,氧氣通過D除去可能存在的CO2,通過B除去水蒸氣,得到純凈干燥的氧氣,氧氣氧化乙醇的條件是需要加熱且有銅做催化劑,因此需要加熱k使乙醇揮發,并且加熱m,使氧氣與乙醇蒸氣反應,反應的化學方程式是:2CH3CH2OH+O2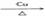 2CH3CHO+2H2O。
2CH3CHO+2H2O。
(3)氫氧化鈉固體易吸水并且在溶于水時放出大量的熱,氫氧化鈉溶于水后溶液中的OH-的濃度增大,這些因素均能濃氨水中的化學平衡:NH3+H2O NH3·H2O
NH3·H2O NH4++OH-向逆反應方向移動,使濃氨水中的氨氣放出。根據常識可以判斷出在E中出現的紅棕色氣體應該是NO2
,由氨氣和NO2中氮元素的化合價可以判斷氨氣被氧化生成NO2
氨氣體現出的是還原性。
NH4++OH-向逆反應方向移動,使濃氨水中的氨氣放出。根據常識可以判斷出在E中出現的紅棕色氣體應該是NO2
,由氨氣和NO2中氮元素的化合價可以判斷氨氣被氧化生成NO2
氨氣體現出的是還原性。
9.8×109g x y
則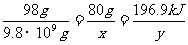 ,解得x=8.0×103t y=9.83×109kJ。
,解得x=8.0×103t y=9.83×109kJ。
36.(07年寧夏理綜·31A)化學選考題(15分)
A.[化學-選修化學與技術]
工業上生產硫酸時,利用催化氧化反應將SO2 轉化為SO3是一個關鍵步驟。壓強及溫度對SO2轉化率的影響如下表(原料氣各成分的體積分數為:SO2 7% O2 11% N2 82%);
 |
0.1 |
0.5 |
1 |
10 |
|
400 |
99.2 |
99.6 |
99.7 |
99.9 |
|
500 |
93.5 |
96.9 |
97.8 |
99.3 |
|
600 |
73.7 |
85.8 |
89.5 |
96.4 |
(1) 已各SO2的氧化是放熱反應,如何利用表中數據推斷此結論?
;
(2)在大400~500℃時,SO2的催化氧化采用常壓而不是高壓,主要原因是:
;
(3)選擇適宜的催化劑,是否可以提高SO2的轉化率? (填“是”或“否”),是否可以增大該反應所放出的熱量? (填“是”或“否”);
(4)為提高SO3吸收率,實際生產中用 吸收SO3;
(5)已知:2SO2(g)+O2(g)=2SO3(g);△H=-196.9kJ·mol-1,計算每生產1萬噸98%硫酸所需要的SO3質量和由SO2生產這些SO3所放出的熱量。
答案:(1)壓強一定時,溫度升高時,SO2轉化率下降,說明升溫有利逆反應的進行,所以正反應為放熱反應。(2)增大壓強對提高SO2轉化率無顯著影響,反而會增加成本。(3)否 否 (4)濃硫酸 (5)8.0×103t 9.83×109kJ
解析:(1)根據表格中的數據可以看出,在相同壓強下(如在0.1MPa下)升高溫度(如由400℃升高到500℃)時SO2的轉化率降低(由99.2%降低為93.5%),即升高溫度時此化學平衡向逆反應方向移動,而升高溫度化學平衡應該向吸熱反應方向移動,所以此反應的正反應為放熱反應。
(2)根據表格中的數據可以得知:在0.1MPa(即常壓1atm下)SO2的轉化率已經很高,如在400℃時已達99.2%,若增大壓強到10MPa(即100atm),壓強增大了100倍但是SO2的轉化率值增大為99.9%,只增大了0.7%變化不大。而壓強增大100倍,需要對設備的材料、動力、能源等都作相應的提高,既要增大成本投入。
(3)使用催化劑只能改變化學反應的速率,改變反應到達平衡的時間,不能使化學平衡發生移動,即對SO2的轉化率不產生影響;而在一定條件下,化學反應放出的熱量與參加反應的反應物的量成正比,因SO2的轉化率不變,所以反應放出的熱量也不會增大。
(4)在生產實際中是采用98.3%的濃硫酸作吸收劑來吸收SO3的。因為若用水進行吸收會形成酸霧,將影響SO3的吸收速率和效率。
(5)1萬噸98%的硫酸含H2SO4的質量:9.8×109g。 設需要SO3的質量為x,該反應產生的熱量為y。
H2SO4 - SO3 - 放出的熱量
98g 80g 196.9kJ
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com