
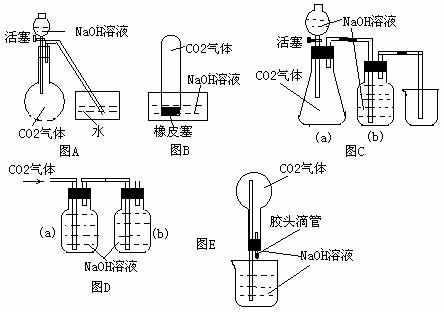
22.(14分)設計一個實驗,能通過觀察到的明顯現象,說明CO2與NaOH溶液發生了反應。實驗用品:集氣瓶、燒瓶、分液漏斗、導管、橡皮管、彈簧夾、燒杯、量筒、水、CO2氣體、NaOH溶液以及你認為所能用到的儀器和藥品。現有五位同學設計了如圖A-E五個裝置,試回答:
(1)對圖A,當將分液漏斗中的NaOH溶液滴入燒瓶時,如果看到水槽中的水被吸入到燒瓶中,則證明CO2與NaOH溶液發生了反應。請寫出NaOH溶液與過量CO2反應的化學方程式:
(2)若用100mL 1mol/LNaOH溶液吸收0.06 mol CO2,所得溶液中的CO32-和HCO3-的物質的量濃度之比為 。
(3)設NA為阿伏加德羅常數,下列關于0.2mol/L的Na2CO3溶液說法不正確的是
A.2L溶液中陰陽離子總數為0.8NA
B.500mL溶液中CO32-離子濃度為0.2mol/L
C.500mL溶液中Na+離子濃度為0.2mol/L
D.500mL溶液中CO32-物質的量為0.4NA
(4)對圖B-E,請指出能達到實驗目的的裝置 (用B、C、D、E填空),并選出其中兩種,說明能證明CO2與NaOH溶液發生了反應的操作及實驗現象,將結果填入下表:
|
所選裝置 |
操作方法 |
實驗現象 |
 |
|
|
21.(13分)將250C 101KPa條件下的氯化氫(HCl)氣體49.6L,通入492mL水中,(已知水的密度為:1.00g/mL),得到密度為1.13g/mL的鹽酸(即氯化氫的水溶液)。注:250C 101KPa條件下氣體摩爾體積為24.8L/mol。(計算結果保留一位小數)
(1)求此鹽酸的質量分數?(5分)
(2)求此鹽酸的物質的量濃度?(5分)
(3)取出20.0 mL該溶液,配成濃度為1.00 mol/L的稀溶液,則稀釋后溶液的體積是多少毫升?(3分)
第Ⅲ卷(附加題 共14分)
20.(10分)現有m g某氣體,它由雙原子分子構成,它的摩爾質量為M g·mol-1。若阿伏加德羅常數用NA表示,則:
(1)該氣體的物質的量為________________mol。
(2)該氣體所含原子總數為________________個。
(3)該氣體在標準狀況下的體積為_________________L。
(4)該氣體在標準狀況下的密度為_______________ g/L。
(5)該氣體溶于水后形成VL溶液,其溶液的物質的量濃度為________________mol/L。
19.(1)(6分)CCl4和蒸餾水都是無色液體,請按下列要求用實驗方法鑒別之(簡要地寫出實驗過程)
① 只允許用一種試劑
② 不用任何試劑
(2)(3分)NaCl溶液中含有少量的CaCl2,某學生用過量的Na2CO3使Ca2+離子轉化為沉淀而除去,確認Na2CO3已過量的實驗方法是
18.(14分)實驗室用NaOH固體配制250mL 1.25mol/L的NaOH溶液,填空并請回答下列問題:
(1)配制250mL 1.25mol/L的NaOH溶液
|
應稱取NaOH的質量/g |
應選用容量瓶的規格/mL |
除容量瓶外還需要的其它儀器 |
|
|
|
|
(2)容量瓶上需標有以下五項中的 ;A
①溫度 ②濃度 ③容量 ④壓強 ⑤刻度線
(3)配制時,其正確的操作順序是(字母表示,每個字母只能用一次) ;
A、用30mL水洗滌燒杯2-3次,洗滌液均注入容量瓶,振蕩
B、用天平準確稱取所需的NaOH的質量,加入少量水(約30mL),用玻璃棒慢慢攪動,使其充分溶解
C、將已冷卻的NaOH溶液沿玻璃棒注入250mL的容量瓶中
D、將容量瓶蓋緊,顛倒搖勻
E、改用膠頭滴管加水,使溶液凹面恰好與刻度相切
F、繼續往容量瓶內小心加水,直到液面接近刻度1-2cm處
(4)操作A中,將洗滌液都移入容量瓶,其目的是 ,溶液注入容量瓶前需恢復到室溫,這是因為_____________________________;
(5)下列配制的溶液濃度偏低的是 ;
A、稱量NaOH時,砝碼錯放在左盤
B、向容量瓶中轉移溶液時(實驗步驟②)不慎有液滴灑在容量瓶外面
C、加蒸餾水時不慎超過了刻度線
D、定容時俯視刻度線
E、配制前,容量瓶中有少量蒸餾水
16.(6分)把下面所列實例填入表中相對應的位置
|
分離和提純方法 |
過程 |
實例 |
|
傾洗 |
用液體分離密度相差較大且不溶的固體 |
|
|
過濾 |
從液體中分離不溶的固體 |
|
|
結晶 |
從溶液中分離已溶解的溶質 |
|
|
蒸餾 |
從溶液中分離溶劑和非揮發性溶質 |
|
|
萃取 |
加入適當溶劑把混合物中某成分溶解及分離 |
|
|
吸附 |
除去混合物中的氣態或固態雜質 |
|
A、大米中混有沙子
B、做豆腐時,將豆腐花與豆漿水分離
C、從酒水中制取濃度較大的酒
D、用活性炭除去冰箱內的臭味
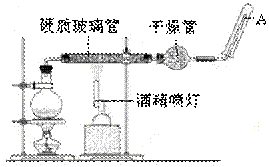 E、不慎灑在衣服上的油湯用酒精除去
E、不慎灑在衣服上的油湯用酒精除去
F、從海水中提取食鹽
|
|
(1)該反應的化學方程式為:3 Fe + 4 H2O ==== Fe3O4 + 4 H2↑;請指出該氧化還原反應的還原劑是 。
(2)實驗前必須對整套裝置進行氣密性檢查,操作方法是 。
(3)圓底燒瓶中盛裝了水,燒瓶底部放置了幾片碎瓷片,碎瓷片的作用是 。
(4)酒精燈和酒精噴燈點燃的順序是 。
(5)干燥管中盛裝的物質是 ,作用是 。
(6)試管中收集的氣體是 ,如果要在A處玻璃管點燃該氣體,則必須對該氣體進行 。
15.(8分)如右圖所示a、b、c、d分別是幾種常見漏斗的上部,A、B、C、D是實際操作中各漏斗的下部插入容器中的示意圖,請指出A、B、C、D分別與a、b、c、d相匹配的組合及其組合后裝置在實驗中的應用,例如:C和a組合,用于制取氣體。
(1)A與 組合,用于 ,
(2)B與 組合,用于 ,
(3)B與 組合,用于 ,
(4)D與 組合,用于 。
14.標準狀況下,①6.72L NH3 ②1.204×1023個 H2S ③5.6g CH4 ④0.5mol HCl ,下列關系正確的是
A.體積大小:④>③>②>① B.原子數目:③>①>④>②
C.密度大小:④>②>③>① D.質量大小:④>③>②>①
第Ⅱ卷(非選擇題 共72分)
13.下列條件下,兩瓶氣體所含原子數一定相等的是
A.同質量、不同密度的N2和CO
B.同溫度、同體積的H2和N2
C.同體積、同密度的C2H4和C3H6
D.同壓強、同體積的N2O和CO2
12.已知某溶液的:①體積;②密度;③溶質和溶劑的質量比;④溶質的摩爾質量,要根據溶質的溶解度計算其飽和溶液的物質的量濃度時,上述條件中必不可少的是
A.①②③④ B.①②③
C.②④ D.①④
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com