
 2NaHCO3 Na2CO3+CO2↑+H2O
2NaHCO3 Na2CO3+CO2↑+H2O
(1)碳酸氫銨與飽和食鹽水反應,能析出碳酸氫鈉晶體的原因是 (填字母標號)。
a.碳酸氫鈉難溶于水 b.碳酸氫鈉受熱易分解
c.碳酸氫鈉的溶解度相對較小,所以在溶液中首先結晶析出
(2)某探究活動小組根據上述制堿原理,進行碳酸氫鈉的制備實驗,同學們按各自設計的方案實驗。
① 一位同學將二氧化碳氣體通入含氨的飽和食鹽水中制備碳酸氫鈉,實驗裝置如下圖所示(圖中夾持、固定用的儀器未畫出)。
22.(12分)我國化工專家侯德榜的“侯氏制堿法”曾為世界制堿工業做出了突出貢獻。他以NaCl、NH3、CO2等為原料先制得NaHCO3,進而生產出純堿。有關反應的化學方程式為:NH3+CO2+H2O NH4HCO3 ;
NH4HCO3+NaCl NaHCO3↓+NH4Cl ;
21.(12分)A、B、C是中學化學中常見的三種短周期元素。已知①A元素原子最外層電子數是次外層電子數的2倍。②B元素最高正價與負價的代數和為2。③C元素有多種化合價,且常溫下C元素的單質與某種一元堿溶液反應,可得到兩種含C元素的化合物。④B、C兩種元素質子數之和是A元素質子數的4倍。
( 1 ) 寫出A、B、C三種元素的名稱:A B C
( 2 ) 寫出C的單質和強堿溶液反應的離子方程式 。
(3)由B、C兩種元素組成的化合物X,常溫下為易揮發的淡黃色液體,X子為三角錐形分子,且分子里B、C兩種原子最外層均達到8個電子的穩定結構。X遇水蒸氣可形成一種常見的漂白性物質。則X的分子式 。分子中B、C原子間的化學鍵的類型為 。(填“極性鍵”或“非極性鍵”)X與水反應的化學方程式 。
(4)A、B兩種元素可形成一種硬度比金剛石還大的化合物Y。在化合物Y中,A、B兩原子以單鍵相結合,且每個原子的最外層均達到8個電子的穩定結構。則Y的化學式為 , Y的硬度比金剛石硬度大的原因是 。
20.硝酸銨(NH4NO3)在不同條件下分解可以得到不同的產物,下列各組物質中肯定不可能是硝酸銨分解產物的是
A.N2O、H2O B.N2、O2、H2O
C.N2、HNO3、H2O D.NH3、NO、H2
2007高三化學周考測試題
第Ⅱ卷(非選擇題,共40分)
題號
1
2
3
4
5
6
7
8
9
10
答案
題號
11
12
13
14
15
16
17
18
19
20
答案
A.V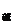 = 102 V
= 102 V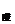 B.V
B.V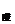 = 102V
= 102V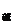 C.V
C.V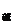 =2V
=2V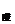 D.V
D.V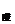 =2 V
=2 V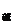
19、室溫下,某強酸溶液pH = a,某強堿溶液pH = b,已知a
+ b = 12,且兩溶液混合后溶液pH = 7。則該強酸溶液的體積V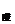 與強堿溶液的體積V
與強堿溶液的體積V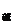 的正確關系為
的正確關系為
D.Ca2+的結構示意圖為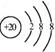 ,NH4Cl的電子式為
,NH4Cl的電子式為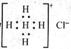
18.正確掌握化學用語和化學基本概念是學好化學的基礎。下列有關表述中正確的一組是
A.過氧乙酸(CH3COOOH)與羥基乙酸(HOCH2COOH)所含官能團相同;兩者互為同分異構體
B.16O與18O互為同位素;H216O、D216O、H218O、D218O互為同素異形體
C.P4、CH4、NH4+粒子的空間構型均為正四面體型;CO2、C2H2均為直線型分子
17.從海水中提取鎂,可按如下步驟進行:
①把貝殼制成石灰乳; ②在引入的海水中加入石灰乳,沉降、過濾、洗滌沉淀物; ③將沉淀物與鹽酸反應,結晶過濾、在HCl氣體氛圍中干燥產物; ④將得到的產物熔融電解得到鎂。下列說法不正確的是
A.此法的優點之一是原料來源豐富
B.①②③步驟的目的是從海水中提取MgCl2
C.以上提取鎂的過程中涉及化合、分解和復分解反應
D.第④步電解時陰極產生氯氣
 Z
Z
例
氧化物
化合物
純凈物
A
苯的同系物
芳香烴
芳香族化合物
B
膠體
分散系
混合物
C
電解質
離子化合物
化合物
D
堿性氧化物
金屬氧化物
氧化物
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com