
| A. | 向某固體中加入稀鹽酸有氣泡產生,可證明該物質中一定含有CO32- | |
| B. | 可用過量的Cu(OH)2除去CuSO4溶液中少量的H2SO4 | |
| C. | 常溫下可用Fe與AgCl反應制取Ag | |
| D. | 將Fe、Cu、Ag放入稀鹽酸中,可確定它們的活動性順序 |
分析 A、碳酸鹽、活潑金屬分別與稀鹽酸反應均能放出二氧化碳與氫氣;
B、氫氧化銅不溶于水但能與稀硫酸反應生成硫酸銅和水;
C、金屬與鹽反應需要滿足:單質金屬的活動性比鹽中金屬活動性強、鹽為可溶性鹽;
D、將Fe、Cu、Ag放入稀鹽酸中,鐵可與鹽酸反應,而銅、銀不能與鹽酸反應.
解答 解:A、活潑金屬也可與鹽酸反應放出氣體氫氣,因此向某固體中加入稀鹽酸有氣泡產生,在未證明氣體為二氧化碳時,不能證明該物質中一定含有CO32-,故A不正確;
B、向混有少量的H2SO4的CuSO4溶液中加入過量的Cu(OH)2,氫氧化銅與硫酸反應生成硫酸銅和水,在除去硫酸同時不引入新雜質,可達到除去雜質的目的,故B正確;
C、由于氯化銀不溶于水,因此雖然鐵的活動性比銀強,但鐵卻不能與氯化銀反應而得到銀,故C不正確;
D、分別將Fe、Cu、Ag放入稀鹽酸中,由于Fe可與鹽酸反應而Cu、Ag不能與鹽酸反應,無法判斷Cu、Ag的活動性順序,故D不正確.
故選B.
點評 金屬與酸反應時,在金屬活動性順序中位于氫前的金屬可與酸發生放出氫氣;金屬與鹽反應時,既要考慮金屬活動性強弱還要考慮鹽的可溶性.


 活力課時同步練習冊系列答案
活力課時同步練習冊系列答案科目:初中化學 來源: 題型:實驗探究題
| 操作 | 現象 | 結論 | 裝置 |
| 實驗一: 同時將Ⅰ中5mL5%的過氧化氫溶液和Ⅱ中5mL15%的過氧化氫溶液注入各盛有0.5g二氧化錳的甲、乙中,關閉彈簧夾. | 發現燒杯中右側導管口產生氣泡的速率比左側快. | 化學反應速率與 反應物濃度有關; 該反應的化學方程式為 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑. | 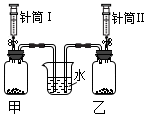 |
| 操作 | 現象 | 現象分析 | 裝置 |
| 實驗二: 先將稀鹽酸注入甲,關閉彈簧夾;再將水注入乙,關閉彈簧夾. 注意:注入液體后,甲、乙導管口均處于液面以下. | 甲中液體先流入燒杯,乙中液體后流入燒杯,然后觀察到燒杯中先無明顯現象,后有白色沉淀產生. | 乙中液體流入燒杯的原因是 氫氧化鈉溶于水,放出熱量,使得瓶內壓強大于外界壓強; 甲中流入燒杯的液體溶質的化學式是 MgCl2HCl. | 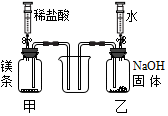 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 磷加氧氣生成五氧化二磷 | |
| B. | 磷和氧氣混合后生成五氧化二磷 | |
| C. | 4個磷原子加10個氧原子等于2個五氧化二磷分子 | |
| D. | 4個磷原子與5個氧分子在點燃條件下反應生成2個五氧化二磷分子 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 反應①說明SO2與CO2有相似的化學性質 | |
| B. | 反應②的反應類型是化合反應 | |
| C. | 反應③說明NaHSO3屬于酸 | |
| D. | 以上反應說明Na2SO3與NaHSO3可相互轉化 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 開發高效氫能,太陽能等新型電動汽車,以解決城市機動車尾氣排放問題 | |
| B. | 塑化劑是一種應用很廣的化工塑料軟化劑,可大量添加到食品中 | |
| C. | 航天員太空實驗能夠證明水分子組成和結構在太空中發生改變 | |
| D. | 汽油標準已由“國Ⅲ”提到“國Ⅳ”,這意味著汽車不再排放氮氧化物 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 80℃時,A飽和溶液與B飽和溶液相比,前者所含溶質的質量一定比后者小 | |
| B. | 30℃時,若A的溶解度比B大,則m一定小于n | |
| C. | 30℃時,若A的溶解度比B小,則m一定大于n | |
| D. | 30℃時,A飽和溶液與B飽和溶液相比,后者溶質的質量分數一定比前者大 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com