
科目: 來源: 題型:選擇題
| A. | 甲基-CH3 | B. | 羥基-OH- | C. | 醛基-CHO | D. | 羧基-COOH |
查看答案和解析>>
科目: 來源: 題型:解答題
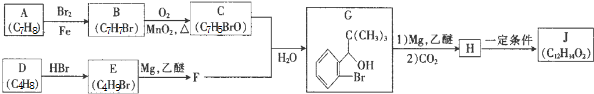
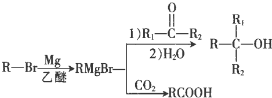
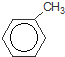 +Br2$\stackrel{鐵粉}{→}$
+Br2$\stackrel{鐵粉}{→}$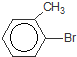 +HBr.,其反應(yīng)類型為取代反應(yīng);
+HBr.,其反應(yīng)類型為取代反應(yīng);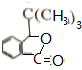 ,由D生成E的化學(xué)反應(yīng)方程式為CH2=C(CH3)2+HBr→(CH3)3CBr;
,由D生成E的化學(xué)反應(yīng)方程式為CH2=C(CH3)2+HBr→(CH3)3CBr;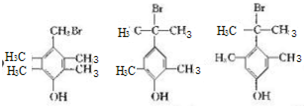 (其中一種)(寫出一種即可).
(其中一種)(寫出一種即可).查看答案和解析>>
科目: 來源: 題型:解答題
 太陽能電池是通過光電效應(yīng)或者光化學(xué)效應(yīng)直接把光能轉(zhuǎn)化成電能的裝置.其材料除單晶硅,還有銅銦鎵硒等化合物.
太陽能電池是通過光電效應(yīng)或者光化學(xué)效應(yīng)直接把光能轉(zhuǎn)化成電能的裝置.其材料除單晶硅,還有銅銦鎵硒等化合物.查看答案和解析>>
科目: 來源: 題型:解答題
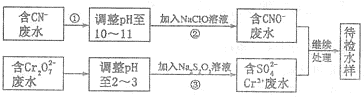
查看答案和解析>>
科目: 來源: 題型:解答題
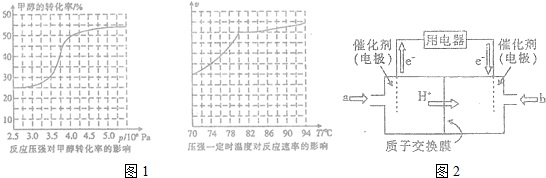
查看答案和解析>>
科目: 來源: 題型:解答題
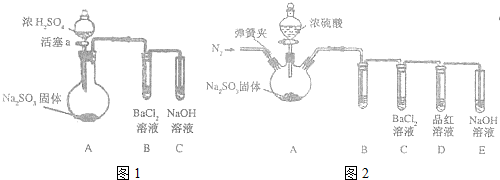
查看答案和解析>>
科目: 來源: 題型:解答題
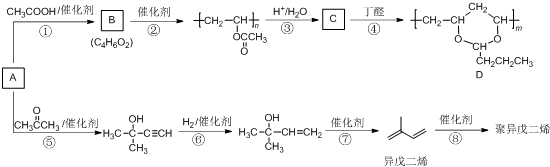
查看答案和解析>>
科目: 來源: 題型:解答題
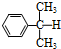 )氧化法是工業(yè)生產(chǎn)苯酚和丙酮最主要的方法.其反應(yīng)和流程如下:
)氧化法是工業(yè)生產(chǎn)苯酚和丙酮最主要的方法.其反應(yīng)和流程如下: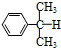 +O→
+O→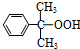 (異丙苯過氧氫)
(異丙苯過氧氫)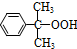 $→_{50-60℃}^{H+}$
$→_{50-60℃}^{H+}$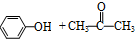 (丙嗣)
(丙嗣)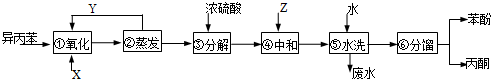
| 物質(zhì) | 丙酮 | 苯酚 | 異丙苯 |
| 密度(g/mL) | 0.7898 | 1.0722 | 0.8640 |
| 沸點(diǎn)/°C | 56.5 | 182 | 153 |
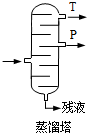 ,產(chǎn)品T是丙酮,
,產(chǎn)品T是丙酮, ;第1加鹽酸、第②步加KI溶液,要迅速蓋好蓋子的原因是溴易揮發(fā).
;第1加鹽酸、第②步加KI溶液,要迅速蓋好蓋子的原因是溴易揮發(fā).查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺 | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com