
分析 Ⅰ、(1)評價實驗方案要從反應的可操作性,生成物的性質,環保節能等方面分析.由于硝酸與銅直接反應時會生成有毒的氮氧化物,第一個方案環保并且使用的硫酸量較小進行分析;
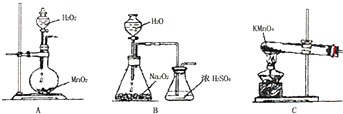
(2)實驗時通入O2的速率不宜過大,為便于觀察和控制產生O2的速率,分析裝置可知,利用分液漏斗控制加入水的量,觀察濃硫酸中氣泡的快慢知道產生氧氣的速率;
(3)根據(2)的分析可知,產生氧氣是用過氧化鈉與水反應,產物除了氧氣外還有氫氧化鈉;
Ⅱ、(1)如果假設1成立,則氧化銅與稀硫酸反應生成硫酸銅溶液,硫酸銅溶液呈藍色,滴加KSCN溶液后溶液無明顯變化;
(2)如果假設2成立,Fe3O4與稀硫酸反應生成硫酸鐵和硫酸亞鐵的混合溶液,三價鐵離子遇到KSCN顯血紅色,亞鐵離子能使高錳酸鉀溶液褪色,據此可以檢驗亞鐵離子的存在;
(3)如果假設3成立,CuO和Fe3O4的混合物溶于稀硫酸生成硫酸鐵和硫酸亞鐵及硫酸銅混合溶液,加和足量的鐵粉,鐵粉與銅離子反應置換出銅,同時鐵粉與過量的稀硫酸反應會產生氫氣,據此答題.
解答 解:Ⅰ、(1)甲方案中放出的有毒氣體氮氧化物會造成對空氣的污染,因此,從保護環境的角度來看,甲方案不合理;乙方案銅和氧氣加熱生成氧化銅,氧化銅和硝酸反應產生硝酸銅和水,因此反應過程中沒有污染物,且原料的利用率高;
故答案為:乙;甲方案會生成污染環境的SO2氣體,乙方案則沒有SO2氣體生成;
(2)實驗時通入O2的速率不宜過大,為便于觀察和控制產生O2的速率,分析裝置可知,利用分液漏斗控制加水的量能達到要求,裝置B中生成的氧氣通過濃硫酸可以干燥氧氣,同時觀察氣體氣泡冒出的速率控制生成氧氣的速率,所以選擇B裝置;
故答案為:B;
(3)根據(2)的分析可知,產生氧氣是用過氧化鈉與水反應,產物除了氧氣外還有氫氧化鈉,反應的方程式為2Na2O2+2H2O=4NaOH+O2↑,
故答案為:2Na2O2+2H2O=4NaOH+O2↑;
Ⅱ、(1)如果假設1成立,則氧化銅與稀硫酸反應生成硫酸銅溶液,硫酸銅溶液呈藍色,滴加KSCN溶液后溶液無明顯變化,
故答案為:藍;
(2)如果假設2成立,Fe3O4與稀硫酸反應生成硫酸鐵和硫酸亞鐵的混合溶液,三價鐵離子遇到KSCN顯紅色,所以反應現象為溶液變為紅色,亞鐵離子能使高錳酸鉀溶液褪色,所以檢驗亞鐵離子的方法是取X溶液少許于試管中,向其中滴加少量的酸性KMnO4溶液,若KMnO4褪色則證明X溶液中含有Fe2+離子,反之則不含,
故答案為:溶液變為紅色;取X溶液少許于試管中,向其中滴加少量的酸性KMnO4溶液,若KMnO4褪色則證明X溶液中含有Fe2+離子,反之則不含;
(3)如果假設3成立,CuO和Fe3O4的混合物溶于稀硫酸生成硫酸鐵和硫酸亞鐵及硫酸銅混合溶液,加和足量的鐵粉,鐵粉與銅離子反應置換出銅,同時鐵粉與過量的稀硫酸反應會產生氫氣,所以實驗現象為溶液X中會有氣泡冒出,且紅色的沉淀生成,
故答案為:溶液X中會有氣泡冒出,且紅色的沉淀生成.
點評 本題考查了物質成分探究實驗,題目涉及的知識點比較多,可以根據信息及所學知識,合理分析得出正確結論,本題難度中等,分析一個反應的可行性要從多方面分析,如從反應的可行性,環保安全,操作簡便,經濟節能方面考慮.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Al→Al2O3→Al(OH)3→AlCl3 | B. | Fe→FeCl3→Fe(OH)3→Fe2O3 | ||
| C. | Mg→MgCl2→Mg(OH)2→MgSO4 | D. | Na→NaOH→Na2CO3→NaCl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 正反應為放熱反應 | |
| B. | 圖中P點:v(正)>v(逆) | |
| C. | 950℃時,0~1.25s生成H2的平均反應速率為:0.016mol•L-1•s-1 | |
| D. | 950℃時,該反應的平衡常數的值小于3.125×10-4 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
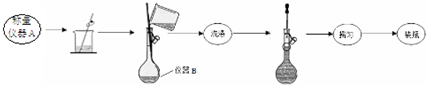
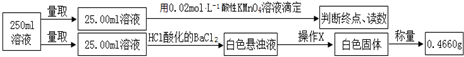
| 實驗次數 | 第一次 | 第二次 | 第三次 |
| 消耗高錳酸鉀溶液體積/mL | 10.32 | 10.02 | 9.98 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2.0gH218O與D20的混合物中所含中子數為NA | |
| B. | 等物質的量的水與重水含有的中子數相等 | |
| C. | 18gD20和18gH20中含有的質子數均為10NA | |
| D. | 235g核素$\left.\begin{array}{l}{235}\\{92}\end{array}\right.$U發生裂變反應:$\left.\begin{array}{l}{235}\\{92}\end{array}\right.$U+$\left.\begin{array}{l}{1}\\{0}\end{array}\right.$n$\frac{\underline{\;裂變\;}}{\;}$$\left.\begin{array}{l}{90}\\{38}\end{array}\right.$Sr+$\left.\begin{array}{l}{136}\\{54}\end{array}\right.$U+10$\left.\begin{array}{l}{1}\\{0}\end{array}\right.$n凈產生的中子($\left.\begin{array}{l}{1}\\{0}\end{array}\right.$n)數為10NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 若金屬有剩余,在溶液中再滴入硫酸后,金屬不溶解 | |
| B. | 若金屬全部溶解,則溶液中一定含有Fe3+ | |
| C. | 若金屬全部溶解,則溶液中一定含有Fe2+ | |
| D. | 若金屬有剩余,不可能只有鐵 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分液時,分液漏斗中的兩層液體均從下口放出 | |
| B. | 蒸發操作時,應使混合物中的水分完全蒸干后,才能停止加熱 | |
| C. | 稱量NaOH固體時,將NaOH固體放在托盤天平左盤的紙上 | |
| D. | 不慎將濃堿沾到皮膚上,應立即用大量水沖洗,然后涂上硼酸溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com