
分析 (1)表示強酸與強堿反應生成可溶性鹽和水的反應;
(2)該反應表示可溶性銅鹽與可溶性強堿反應生成氫氧化銅和可溶性鹽的反應.
解答 解:(1)OH-+H+═H2O表示強酸與強堿反應生成可溶性鹽和水的反應,如:NaOH+HCl=NaCl+H2O,
故答案為:NaOH+HCl=NaCl+H2O;
(2)Cu2++2OH-═Cu(OH)2↓表示可溶性銅鹽與可溶性強堿反應生成氫氧化銅沉淀和可溶性鹽的一類反應,如:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4,
故答案為:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4.
點評 本題考查離子反應方程式的書寫,為高頻考點,把握離子反應方程式的意義及離子反應的書寫方法為解答的關鍵,側重分析與應用能力的考查,題目難度不大.


科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
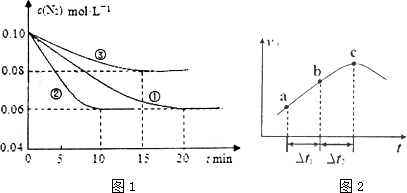
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 以高純H2為燃料的質子交換膜燃料電池具有能量效率高、無污染等優點,但燃料中若混有CO將顯著縮短電池壽命.以甲醇為原料制取高純H2是重要研究方向.
以高純H2為燃料的質子交換膜燃料電池具有能量效率高、無污染等優點,但燃料中若混有CO將顯著縮短電池壽命.以甲醇為原料制取高純H2是重要研究方向.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
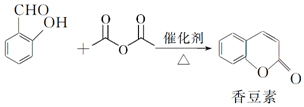
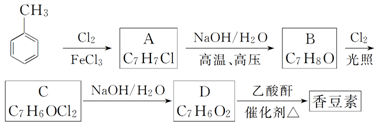
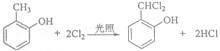 ;
;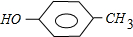 和
和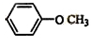 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 若忽略水的電離及H2CO3的第二級電離,則H2CO3?HCO3-+H+的平衡常數K1=4.2×10-7 | |
| B. | 少量Cl2通入到過量的Na2CO3溶液的離子方程式為Cl2+2CO32-+H2O═2HCO3-+Cl-+ClO- | |
| C. | Cl2與Na2CO3按物質的量之比1:1恰好反應的離子方程式為Cl2+CO32-+H2O═HCO3-+Cl-+HClO | |
| D. | 少量CO2通入到過量的NaClO溶液的離子方程式為2ClO-+CO2+H2O═CO32-+2HClO |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com