
分析 ①根據化學式中原子數計算;
②同溫同壓下,體積之比等于物質的量比等于分子數之比;
③根據分子中H原子數計算;
④根據分子中含有的碳原子數計算.
解答 解:①0.1molFe2(SO4)3中含Fe3+的物質的量為0.2mol,其鐵離子的數目為0.2NA;故答案為:0.2NA;
②同溫同壓下,體積之比等于物質的量比等于分子數之比,則等體積的CH4和C2H6兩種氣體所含分子數之比為1:1;
故答案為:1:1;
③等體積的CH4和C2H6兩種氣體所含分子數之比為1:1,則H原子數之比為4:6=2:3;
故答案為:2:3;
④等體積的CH4和C2H6兩種氣體所含分子數之比為1:1,則含有的碳原子數之比為1:2;
故答案為:1:2.
點評 本題考查了物質的量的計算,題目等濃度,明確物質的量與微粒之間的關系為解答關鍵,試題側重基礎知識的考查,培養了學生的化學計算能力.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
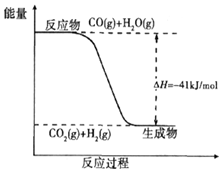 煤炭可以轉化為清潔能源和化工原料.
煤炭可以轉化為清潔能源和化工原料.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 在一定體積的密閉容器中,進行反應:CO2(g)+H2(g)?CO(g)+H2O(g),其反應化學平衡常數和T的關系如表所示:
在一定體積的密閉容器中,進行反應:CO2(g)+H2(g)?CO(g)+H2O(g),其反應化學平衡常數和T的關系如表所示:| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
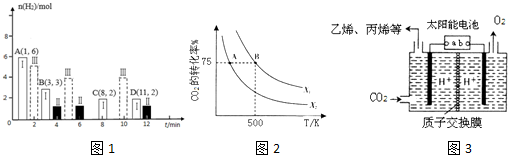
| 化學鍵 | H-H | C-O | C $\frac{\underline{\;←\;}}{\;}$O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 1076 | 465 | x |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲烷的燃燒熱為△H=-890kJ•mol-1,則甲烷燃燒的熱化學方程式可表示為:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890 kJ?mol-1 | |
| B. | 500℃、30 MPa下,將0.5 mol N2和1.5 mol H2置于密閉的容器中充分反應生成NH3(g),放熱19.3 kJ,其熱化學方程式為N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 已知:H2(g)+F2(g)=2HF(g);△H=-270 kJ/mol,則1 mol氫氣與1 mol氟氣反應生成2 mol液態氟化氫放出的熱量小于270 KJ | |
| D. | 在C中相同條件下,2 mol HF氣體的能量小于1 mol氫氣與1 mol氟氣的能量總和 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com