
| 時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)(mol•L-1) | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)(mol•L-1) | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
| 實驗編號 | T(℃) | NO初始濃(mol•L-1) | 催化劑的比表面積(m2•g-1) | NO平衡濃度(mol•L-1) |
| 甲 | 280 | 1.80×10-3 | 82 | 0.60×10-3 |
| 乙 | 280 | 1.80×10-3 | 124 | c(乙) |
| 丙 | T(丙) | 1.80×10-3 | 124 | 0.98×10-3 |
分析 Ⅰ.(1)根據反應能夠自發進行,則△H-T△S<0來分析該反應的焓變;
(2)根據化學反應速率V=$\frac{△c}{△t}$來計算解答;平衡常數指各生成物濃度的化學計量數次冪的乘積除以各反應物濃度的化學計量數次冪的乘積所得的比值,根據該溫度下達化學平衡時各物質平衡時濃度及化學平衡常數的概念來計算;
(3)按化學計量數將已知物質的物質的量轉化到方程式右邊物質,然后進行比較;
(4)該實驗是驗證溫度、催化劑比表面積對化學反應速率的影響規律,所以甲、乙是只改變催化劑表面積,乙、丙只改變溫度;
Ⅱ.根據n=$\frac{m}{M}$計算2gN2H4的物質的量,再根據熱化學方程式書寫原則書寫熱化學方程式;肼-氧氣堿性燃料電池中,負極上燃料肼失電子和氫氧根離子反應生成水和氮氣,用該電池做電源使用惰性電極熔融Na2SO4,電解池中陽極硫酸根離子放電生成三氧化硫和氧氣.
解答 解:Ⅰ.(1)因該反應2NO(g)+2CO(g) 2CO2(g)+N2(g)中氣體減少,△S<0,由反應能夠自發進行,則△H-T△S<0,即該反應一定是放熱才有可能自發進行,放熱反應中△H<0,
2CO2(g)+N2(g)中氣體減少,△S<0,由反應能夠自發進行,則△H-T△S<0,即該反應一定是放熱才有可能自發進行,放熱反應中△H<0,
故答案為:<;
(2)由表格中的數據可知3s內NO濃度的變化量為1.00×10-3-1.50×10-4=8.50×10-4,則υ(NO)=$\frac{8.5×1{0}^{-4}}{3}$mol•L-1•s-1;由化學反應速率之比等于化學計量數之比,則υ(N2)=$\frac{1}{2}$υ(NO)≈1.42×10-4mol•L-1•s-1;
由表格中的數據可知到4s時達到化學平衡,則
2NO+2CO  2CO2 +N2,
2CO2 +N2,
開始(mol/L) 1.00×10-3 3.60×10-3 0 0
轉化(mol/L) 9×10-4 9×10-4 9×10-4 4.50×10-4
平衡(mol/L)1.00×10-4 2.70×10-3 9×10-4 4.50×10-4
則平衡常數K=$\frac{C({N}_{2})×{C}^{2}(C{O}_{2})}{{C}^{2}(NO)×{C}^{2}(CO)}$=$\frac{(4.5×1{0}^{-4})×(9×1{0}^{-4})^{2}}{(1.00×1{0}^{-4})^{2}×(2.7×1{0}^{-3})^{2}}$=5000,
故答案為:1.42×10-4;5000;
(3)按化學計量數將已知物質的物質的量轉化到方程式右邊物質
a.0.1molNO、0.1molCO、0.1molCO2、0.04molN2相當于0.2molCO2、0.09molN2;
b.0.2molNO、0.2molCO 相當于0.2molCO2、0.1molN2;
c.0.21molCO2、0.09molN2;
相同條件下,ab比較,a的N2含量小,ac比較C的N2含量小,
故答案為:C;
(4)該實驗是驗證溫度、催化劑比表面積對化學反應速率的影響規律,則物質的濃度數據相同,只有溫度、接觸面積兩個變量,所以甲、乙是只改變催化劑表面積,c(乙)=0.60×10-3mol•L-1,乙、丙只改變溫度,丙組:NO平衡濃度(mol•L-1)=0.98×10-3>0.60×10-3. 該反應正反應為放熱,所以丙溫度高于甲,
故答案為:>;=;
Ⅱ.2gN2H4的物質的量為$\frac{2g}{32g/mol}$=$\frac{1}{16}$mol,與二氧化氮反應生成氮氣與氣態水放出35.5kJ的熱量,1mol液態肼與足量液態雙氧水反應時放出的熱量16×35.5kJ=568KJ,則熱化學方程式為:2N2H4(g)+2NO2(g)═3N2(g)+4H2O(l)△H=-1136kJ•mol-1,
故答案為:2N2H4(g)+2NO2(g)═3N2(g)+4H2O(l)△H=-1136kJ•mol-1;
肼-氧氣堿性燃料電池中,負極上燃料肼失電子和氫氧根離子反應生成水和氮氣,電極反應式為N2H4+4OH--4e-=4H2O+N2↑,正極發生還原反應,電極方程式為O2+2H2O+4e-=4OH-,若用該電池做電源使用惰性電極熔融Na2SO4,電解池中陽極硫酸根離子放電生成三氧化硫和氧氣,電極反應式為:2SO42--4e-=2SO3+O2↑,
故答案為:O2+2H2O+4e-=4OH-;N2H4+4OH--4e-=4H2O+N2↑;2SO42--4e-=2SO3+O2↑.
點評 本題考查較為綜合,涉及化學平衡的移動,原電池與電解池等知識,題目難度較大,注意把握電極方程式的書寫以及平衡移動原理的應用.


科目:高中化學 來源: 題型:選擇題
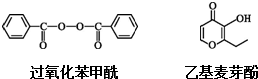
| A. | 過氧化苯甲酰、過氧化鈣漂白原理與SO2漂白原理不同 | |
| B. | 1 mol乙基麥芽酚最多能與3 mol H2發生加成反應 | |
| C. | 上述兩有機物都能發生取代、加成、氧化和還原反應 | |
| D. | 乙基麥芽酚的一種芳香族同分異構體能發生銀鏡反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CuS<Cu(OH)2<CuCO3 | B. | CuS>Cu(OH)2>CuCO3 | C. | Cu(OH)2>CuCO3>CuS | D. | Cu(OH)2>CuCO3>CuS |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 離子交換法淡化海水發生了化學變化 | |
| B. | 海水淡化可為人類提供更多的淡水資源 | |
| C. | 利用太陽能蒸發原理淡化海水屬于物理變化 | |
| D. | 將海水中的鹽分離出來不能達到海水淡化的目的 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 生物柴油是可再生能源 | |
| B. | 發展生物柴油也有益于保護生態環境 | |
| C. | 生物柴油的組成成分與礦物柴油完全相同 | |
| D. | 發展生物柴油有利于調整產業結構、增加農民收入 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com