
(2) 當X=0.5時,平衡后右室SO2的體積分數為a;X=1時,平衡后右室SO2的體積分數為b,則a和b的關系是 ▲ ;
A、a>b B、a=b C、a<b D、無法確定
(3) 若平衡時隔板在中央,則X= ▲ , 左室吸收的熱量為Q1 kJ,右室放出的熱量為Q2 kJ,則Q1、Q2間滿足的關系是 ▲ ;
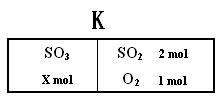
左室:2SO3(g) 2SO2(g) + O2(g) 右室:2SO2(g) + O2(g) 2SO3(g) △H=-197kJ/mol
回答下列問題:
(1) 能說明反應達到平衡的是 ▲ ;
A、隔板不再移動 B、左右二室SO2和O2物質的量之比相等
C、左右兩邊SO2的物質的量相等 D、左右二邊SO3的體積分數相等
17.(10分)如下圖所示,在一定溫度下,在一個容積為
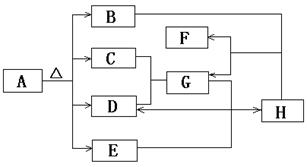
請填寫下列空白:
(1)簡述B形成的酸雨對環境的危害 ▲ ; ▲ (至少二點);
(2)配制F的溶液時要加 ▲ ;
(3)寫出B+H→F+G的離子方程式 ▲ ;
(4)若A分解產生的B、C、D、E的質量比為16∶20∶63∶40,則A的化學式為 ▲ 。
16.(8分)下圖是無機物A~H在一定條件下的轉化關系(部分反應中參加反應的水未列出)。其中,A是一種帶有結晶水的正鹽,B是形成酸雨的主要物質,G是一種常見的二元強酸,E是一種紅棕色粉末。
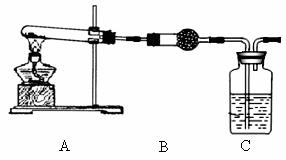
(3)B裝置中試劑的化學式是 ▲ , C裝置中試劑的名稱是 ▲ 。
(4)能證明乙同學觀點正確的實驗現象是 ▲ 。
(5) 若丙同學的觀點正確,用上述裝置通過B、C中質量的增加來定量測定沉淀的組成,請你說說該裝置主要存在的缺點 ▲ (至少二點)
15.某研究性學習小組將一定濃度Na2CO3溶液滴入CuSO4溶液中得到藍色沉淀。
甲同學認為沉淀可能是CuCO3;
乙同學認為沉淀可能是Cu(OH)2;
丙同學認為沉淀可能是CuCO3和Cu(OH)2的混合物。(查閱資料知:CuCO3和Cu(OH)2均不帶結晶水)
Ⅰ.(1)乙同學的觀點,你認為其原理是 ▲ ;
(2)在探究沉淀成分前,須將沉淀從溶液中過濾、洗滌、低溫干燥,檢驗沉淀是否洗滌干凈的方法是 ▲ 。
Ⅱ.請用下圖所示裝置,選擇必要的試劑,定性探究生成物的成分。
14.一定質量的Fe2O3、ZnO、CuO的固體混合粉末,在加熱條件下用足量CO還原,得到金屬混合物4.
A.50 mL B.100 mL C.200 mL D.缺少數據,無法計算
B.將標準狀況下1.
2Fe2++4Br-+3Cl2 =2Fe3++6Cl-+2Br2
C.向NaOH溶液中滴加同濃度的少量Ca(HCO3)2溶液:
Ca2++ HCO3- +OH- =CaCO3↓+H2O
D.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至剛好沉淀完全:
Ba2++2OH-+H++ SO42- + NH4+ =BaSO4↓+ NH3?H2O +H2O
13.下列離子方程式的書寫正確的是
A.實驗室用濃鹽酸與MnO2反應制Cl2:
MnO2 +4HCl(濃) Cl2↑+Mn2+ +2Cl-+2H2O
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com