
科目: 來源: 題型:解答題
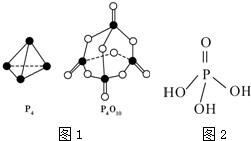
| 化學鍵 | P-P | P-O | P═O | O═O |
| 鍵能/kJ•mol-1 | a | b | c | d |
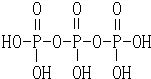 ,三聚磷酸鈉(俗稱“五鈉”)是常用的水處理劑,其化學式為Na5P3O10.
,三聚磷酸鈉(俗稱“五鈉”)是常用的水處理劑,其化學式為Na5P3O10.查看答案和解析>>
科目: 來源: 題型:解答題
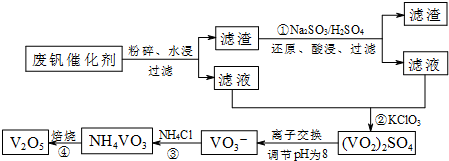
| 物質 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 難溶 | 難溶 | 易溶 |

查看答案和解析>>
科目: 來源: 題型:解答題
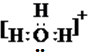 和
和 ;
;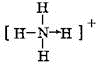 和O=C=O.
和O=C=O.查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 重氫原子:${\;}_{1}^{2}$D | |
| B. | S2-的結構示意圖: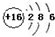 | |
| C. | 質子數為53,中子數為78的碘原子:${\;}_{53}^{131}$I | |
| D. | N2的電子式: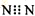 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 朝鮮第三次核試驗產生的放射性物質的衰變為化學變化 | |
| B. | 燃燒化石燃料排放的廢氣中含大量CO2、SO2,形成酸雨 | |
| C. | 為防止垃圾污染城市,可采用露天焚燒或深埋的方法進行處理 | |
| D. | 用高純度二氧化硅制作的光導纖維遇強堿會“斷路” |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | △H=-2 878 kJ•mol-1 | B. | △H=-2 658 kJ•mol-1 | ||
| C. | △H=-1 746 kJ•mol-1 | D. | △H=-1 526 kJ•mol-1 |
查看答案和解析>>
科目: 來源: 題型:實驗題
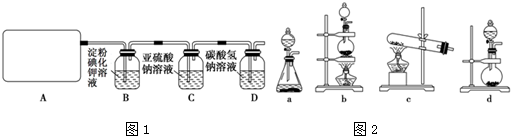
查看答案和解析>>
科目: 來源: 題型:解答題
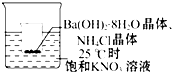 把小燒杯放入25℃的盛有飽和硝酸鉀溶液的大燒杯中,小燒杯(已被設法固定)中放有 25g研成粉末的氫氧化鋇晶體[Ba(OH)2•8H2O],再加入約12g的氯化銨晶體,并攪拌使其充分反應.
把小燒杯放入25℃的盛有飽和硝酸鉀溶液的大燒杯中,小燒杯(已被設法固定)中放有 25g研成粉末的氫氧化鋇晶體[Ba(OH)2•8H2O],再加入約12g的氯化銨晶體,并攪拌使其充分反應.查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | H2燃燒生成1 mol H2O(g)時,放出241.8 kJ的熱量 | |
| B. | O2前面的$\frac{1}{2}$表示參加反應的O2的分子數目 | |
| C. | 燃燒熱是以在101 kPa時,1 mol可燃物完全燃燒生成穩定的氧化物時所放出的熱量定義的,則 H2的燃燒熱為285.8 kJ•mol-1 | |
| D. | 1 mol H2和$\frac{1}{2}$ mol O2所具有的總能量大于1mol H2O(g)所具有的總能量 |
查看答案和解析>>
科目: 來源: 題型:實驗題
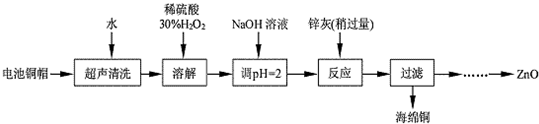
| 實驗編號 | 1 | 2 | 3 | 4 |
| V(Na2S2O3)(mL) | 28.32 | 25.31 | 25.30 | 25.32 |
| 開始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 1.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com