
分析 根據元素符號,判斷元素原子的核外電子數,再根據核外電子排布規律來寫.
解答 解:(1)Fe元素為26號元素,原子核外有26個電子,所以核外電子排布式為:1s22s22p63s23p63d64s2,故答案為:1s22s22p63s23p63d64s2;
(2)Cu元素為29號元素,原子核外有29個電子,所以核外電子排布式為:1s22s22p63s23p63d104s1,故答案為:1s22s22p63s23p63d104s1;
(3)Cr元素為24號元素,原子核外有24個電子,所以核外電子排布式為:1s22s22p63s23p63d54s1,故答案為:1s22s22p63s23p63d54s1;
(4)Si元素為14號元素,原子核外有14個電子,所以核外電子排布式為:1s22s22p63s23p2,故答案為:1s22s22p63s23p2.
點評 本題考查了基態原子的核外電子排布式,核外電子排布規律來寫,題目難度不大.


科目:高中化學 來源: 題型:解答題
| 實驗 編號 | HA物質的量 濃度(mol•L-1) | NaOH物質的量 濃度(mol•L-1) | 混合溶 液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
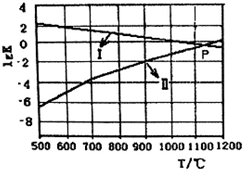 一種煤炭脫硫技術可以把硫元素以CaSO4的形成固定下來,可以減少SO2的排放,但產生的CO又會與CaSO4發生化學反應,從而降低脫硫效率.相關的熱化學方程式如下:
一種煤炭脫硫技術可以把硫元素以CaSO4的形成固定下來,可以減少SO2的排放,但產生的CO又會與CaSO4發生化學反應,從而降低脫硫效率.相關的熱化學方程式如下:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
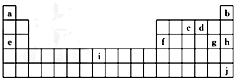
| A. | 原子半徑:A>B>C>D | B. | 原子序數:b>a>c>d | ||
| C. | 離子半徑:D>C>B>A | D. | a+1=d-2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
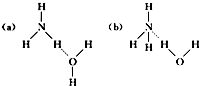
 ,離子鍵,共價鍵;
,離子鍵,共價鍵;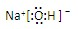 ,離子鍵,共價鍵;
,離子鍵,共價鍵; ;共價鍵;
;共價鍵; ,共價鍵,離子鍵.
,共價鍵,離子鍵.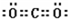 ;共價鍵;
;共價鍵; ;共價鍵.
;共價鍵.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com