
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 672×103L |
| 22.4L/mol |
| 1750×103L |
| 22.4L/mol |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 1 |
| 3 |
| 4 |
| 3 |
| 1 |
| 3 |
| ||
|
| 1 |
| 3 |
| 1 |
| 3 |
| 1 |
| 2 |
| 1 |
| 2 |
| a |
| a+a |


科目:高中化學 來源: 題型:
| A、在溴水中存在如下平衡:Br2+H2O?HBr+HBrO 當加入NaOH溶液后顏色變淺 |
| B、對2HI?H2+I2(g)平衡體系增加壓強使顏色變深 |
| C、反應CO+NO2?CO2+NO△H<0 升高溫度使平衡向逆方向移動 |
| D、合成氨反應:N2+3H2?2NH3,△H<0 為使氨的產率提高,理論上應采取低溫高壓的措施 |
查看答案和解析>>
科目:高中化學 來源: 題型:

| A、常壓下五種元素的單質中Z單質的沸點最高 |
| B、Y、Z的陰離子電子層結構都與R原子的相同 |
| C、W的氫化物還原性小于Y的氫化物 |
| D、Y元素的非金屬性比W元素的非金屬性強 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、同周期元素中X的金屬性最強 |
| B、同周期元素中Y的最高價含氧酸的酸性最強 |
| C、原子半徑X>Y,離子半徑X+>Z2- |
| D、同族元素中Z的氫化物穩定性最高 |
查看答案和解析>>
科目:高中化學 來源: 題型:
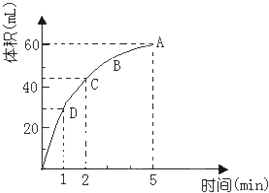 為了研究MnO2與雙氧水(H2O2)的反應速率,某學生加入少許的MnO2粉末于50mL密度為1.1g/cm3的雙氧水溶液中,通過實驗測定:在標準狀況下放出氣體的體積和時間的關系如圖所示.請依圖回答下列問題:
為了研究MnO2與雙氧水(H2O2)的反應速率,某學生加入少許的MnO2粉末于50mL密度為1.1g/cm3的雙氧水溶液中,通過實驗測定:在標準狀況下放出氣體的體積和時間的關系如圖所示.請依圖回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:
| A、7 | B、8 | C、9 | D、10 |
查看答案和解析>>
科目:高中化學 來源: 題型:
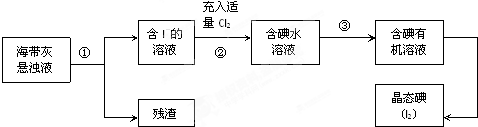
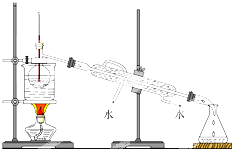
查看答案和解析>>
科目:高中化學 來源: 題型:
A、 I2(g)+H2(g)?2HI(g) |
B、 CH3COOH?H++CH3COO-(忽略溶液體積變化) |
C、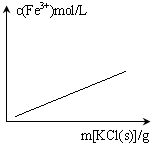 FeCl3+3KSCN?Fe(SCN)3+3KCl(忽略液體體積變化) |
D、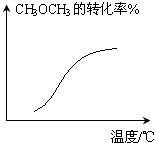 CH3OCH3(g)+3H2O(g)?6H2(g)+2CO(g)-Q(恒壓) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com