
| W | X | Y | Z | |
| 結構或性質 | 最高價氧化物對應的水化物與其氣態氫化物反應得到離子化合物 | 焰色反應呈黃色 | 在同周期主族元素形成的簡單離子中,離子半徑最小 | 最高正價與最低負價之和為零 |

分析 四種短周期元素W、X、Y、Z,原子序數依次增大,W最高價氧化物對應的水化物與其氣態氫化物反應得到離子化合物,則W為N元素;X焰色反應呈黃色,則X為Na;Y、Z原子序數大于Na,二者處于第三周期,在同周期主族元素形成的簡單離子中,Y的離子半徑最小,則Y為Al,Z最高正價與最低負價之和為零,則Z為Si元素,據此解答.
解答 解:四種短周期元素W、X、Y、Z,原子序數依次增大,W最高價氧化物對應的水化物與其氣態氫化物反應得到離子化合物,則W為N元素;X焰色反應呈黃色,則X為Na;Y、Z原子序數大于Na,二者處于第三周期,在同周期主族元素形成的簡單離子中,Y的離子半徑最小,則Y為Al,Z最高正價與最低負價之和為零,則Z為Si元素.
(1)Z是Si元素,處于第ⅣA族,故答案為:ⅣA;
(2)W形成的最高價氧化物的水化物是硝酸,X的最高價氧化物的水化物是氫氧化鈉,Y的最高價氧化物的水化物是氫氧化鋁,Z的最高價氧化物的水化物是硅酸,氫氧化鈉和其他三種物質能反應,所以該元素是Na,故答案為:Na;
(3)①比較金屬性強弱的方法有:金屬元素最高價氧化物的水化物堿性強弱、金屬之間的置換反應、和酸或水反應生成氫氣的難易程度、形成的氯化物溶液酸性強弱等,故選:bc;
②電子層相同,核電荷數Al>Na,原子半徑Na>Al,所以原子核對最外層電子的吸引力Na<Al,失電子能力Na>Al,
故答案為:電子層相同,核電荷數Al>Na,原子半徑Na>Al,所以原子核對最外層電子的吸引力Na<Al,失電子能力Na>Al;
(4)HN3的酸性與醋酸的相當,則HN3為弱酸,與NaOH發生中和反應,反應方程式為:HN3+NaOH═NaN3+H2O;等體積、等濃度,二者恰好反應,為NaN3溶液,NaN3溶液中N3-水解,溶液呈堿性,故溶液中離子濃度順序為c(Na+)>c(N3-)>c(OH-)>c(H+),
故答案為:HN3+NaOH═NaN3+H2O;c(Na+)>c(N3-)>c(OH-)>c(H+);
(5)鎂、鋁和稀硫酸反應生成硫酸鎂、硫酸鋁和氫氣,硫酸鎂、硫酸鋁和氫氧化鈉溶液反應生成氫氧化鎂、氫氧化鋁,氫氧化鋁和氫氧化鈉反應生成偏鋁酸鈉,氫氧化鎂和氫氧化鈉溶液不反應,灼燒氫氧化鎂固體,氫氧化鎂分解生成氧化鎂和水,所以最后所得固體是氧化鎂.
a.根據n的量計算鎂的質量,根據m、n計算鋁質量,從而計算鋁的質量分數,故正確;
b.根據鎂、鋁的質量及鎂鋁和稀硫酸反應生成氫氣的量計算鋁和鎂質量,從而計算鋁的質量分數,故正確;
c.根據n的質量計算鎂的質量,根據鎂的量計算鎂和稀硫酸反應生成氫氣的量,從而得出鋁和稀硫酸反應生成氫氣的量,故而得出鋁的質量分數,故正確,
故選:abc.
點評 本題考查元素周期表及有關推斷、實驗的設計、分析及評價等,推斷元素是解題關鍵,注意掌握金屬性、非金屬性強弱比較實驗事實,難度中等.


 期末沖刺100分創新金卷完全試卷系列答案
期末沖刺100分創新金卷完全試卷系列答案科目:高中化學 來源: 題型:選擇題
| 甲 | 乙 | |
| ① | 物質微粒數 | 阿伏加德羅常數 |
| ② | 標況下氣體摩爾體積 | 標況下氣體體積 |
| ③ | 溶劑的體積 | 溶質的物質的量濃度 |
| ④ | 溶液中溶質的質量分數 | 溶液的質量 |
| ⑤ | 非標況下物質的質量 | 物質的摩爾質量 |
| A. | ③ | B. | ③④ | C. | ②③④ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗步驟 | 實驗方法 | 觀察到的現象 |
| 步驟1 | ||
| 步驟2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
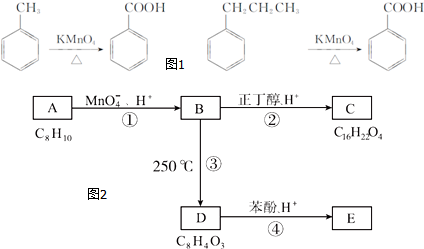
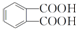 .
.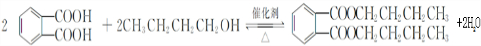 ,該反應的類型為取代反應.
,該反應的類型為取代反應.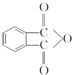 ,在D物質的核磁共振氫譜圖中,會出現2組峰,峰面積之比為1:1.
,在D物質的核磁共振氫譜圖中,會出現2組峰,峰面積之比為1:1.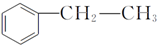 (寫結構簡式).
(寫結構簡式).查看答案和解析>>
科目:高中化學 來源: 題型:解答題
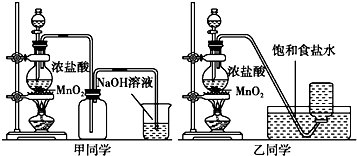
| 實驗序號 | 實驗操作 | 現象 | 結論 |
| ① | 加品紅溶液 | 溶液褪色 | 氯氣與水反應的產物有漂白性 |
| ② | 加入NaHCO2粉末 | 有無色氣泡產生 | 氯氣與水反應的產物具有較強的酸性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Z的氫化物是同主族簡單氫化物中沸點最低的一種 | |
| B. | 非金屬性:Z>Y>X | |
| C. | XY2中各原子最外層均滿足8電子結構 | |
| D. | X、Y、Z的氫化物中化學鍵均為極性共價鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 實驗室所制得的1.7gNH3中含有的電子數為0.1NA | |
| B. | 標準狀況下2.24LHF中含有HF分子數為0.1NA | |
| C. | 1L0.1 mol•L-1NaHSO4溶液中含有的陽離子數目為0.1NA | |
| D. | 0.1mol氯酸鉀與足量鹽酸反應生成氯氣轉移電子數為0.5NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com