
 鐵、銅及其化合物在日常生產、生活有著廣泛的應用.請回答下列問題:
鐵、銅及其化合物在日常生產、生活有著廣泛的應用.請回答下列問題:分析 (1)鐵在元素周期表中的位置是第四周期第VIII族;
(2)分子晶體熔沸點較低;配合物Fe(CO)x的中心原子是鐵原子,其價電子數是8,每個配體提供的電子數是2,據此判斷x值;根據生成物判斷形成的化學鍵;
(3)原子個數相等、價電子數相等的微粒是等電子體;極性分子的熔沸點較高;
(4)①銅為29號元素,據此寫出基態銅原子的核外電子排布式;
②根據晶胞結構圖可知,銅為面心立方堆積,據此判斷每個銅原子周圍距離最近的銅原子數目;
(5)根據價電子排布式判斷出X原子為Cl原子;
①利用均攤法計算得出;
②該晶胞中Cu原子個數為4,Cl原子個數=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,晶體體積=$\frac{\frac{M}{{N}_{A}}×4}{ρ}$cm3,根據晶胞的結構可知,銅原子和M原子之間的最短距離為立方體體對角線的$\frac{1}{4}$.
解答 解:(1)Fe位于第四周期第VIII族,故答案為:第四周期第Ⅷ族;
(2)Fe(CO)x晶體的熔沸點較低,所以屬于分子晶體;Fe原子價電子數是8,每個CO分子提供一個電子對,所以8+2n=18,n=5;只有配位鍵斷裂,生成的物質是Fe,則形成的化學鍵是金屬鍵;
故答案為:分子晶體;5;金屬鍵;
(3)原子個數相等、價電子數相等的微粒是等電子體,所以與CO是等電子體的分子結構式為N≡N;極性分子的熔沸點較高,CO是極性分子,氮氣是非極性分子,所以CO熔沸點較高,
故答案為:N≡N;CO;
(4)①銅為29號元素,基態銅原子的核外電子排布式為[Ar]3d104s1 或1s22s22p63s23p63d104s1,
故答案為:[Ar]3d104s1 或1s22s22p63s23p63d104s1;
②根據晶胞結構圖可知,銅為面心立方堆積,每個銅原子周圍距離最近的銅原子數目=3×8÷2=12,
故答案為:12;
(5)某M原子的外圍電子排布式為3s23p5,則M為Cl元素,
①該晶胞中銅原子個數=4,Cl原子個數=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,所以其化學式為CuCl,故答案為:CuCl;
②該晶胞中Cu原子個數為4,Cl原子個數=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,晶體體積=$\frac{\frac{M}{{N}_{A}}×4}{ρ}$cm3=$\frac{\frac{99.5}{{N}_{A}}×4}{ρ}$cm3=$\frac{99.5×4}{ρ{N}_{A}}$cm3,根據晶胞的結構可知,銅原子和M原子之間的最短距離為立方體體對角線的$\frac{1}{4}$=$\frac{1}{4}$×$\sqrt{3}$×$\root{3}{\frac{99.5×4}{ρ{N}_{A}}}$cm=$\frac{\sqrt{3}}{4}×\root{3}{\frac{99.5×4}{ρ{N}_{A}}}$cm=($\frac{\sqrt{3}}{4}×\root{3}{\frac{99.5×4}{ρ{N}_{A}}}$×1010)pm,故答案為:$\frac{\sqrt{3}}{4}×\root{3}{\frac{99.5×4}{ρ{N}_{A}}}$×1010.
點評 本題考查物質結構和性質,涉及晶胞計算、原子核外電子排布、等電子體、晶體類型判斷等知識點,為高頻考點,難點是晶胞計算,注意(5)②中Cu、Cl原子最短距離與基本棱長關系,題目難度中等.


科目:高中化學 來源: 題型:多選題
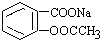 轉變為
轉變為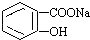 的方法是( )
的方法是( )| A. | 與足量Na0H溶液共熱后,再通入CO2 | |
| B. | 溶液加熱,通入足量的SO2 | |
| C. | 與稀硫酸共熱后,加入足量Na0H溶液 | |
| D. | 足量稀硫酸共熱后,加入足量NaHCO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 在25℃,101KPa的條件下,將共8L的CO和O2的混合氣體通入一個帶可自由移動活塞容積可變但壓強不變的密閉容器中(如圖所示),用電火花點燃充分反應后恢復至原來的條件,測得氣體的密度變為原來的$\frac{4}{3}$,求
在25℃,101KPa的條件下,將共8L的CO和O2的混合氣體通入一個帶可自由移動活塞容積可變但壓強不變的密閉容器中(如圖所示),用電火花點燃充分反應后恢復至原來的條件,測得氣體的密度變為原來的$\frac{4}{3}$,求查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在蒸發皿中放入NaCl溶液,加熱、蒸發所有水分得到NaCl晶體 | |
| B. | 用10 mL的量筒量取5.2 mL的鹽酸 | |
| C. | 用托盤天平稱取25.20 g NaCl | |
| D. | 用1 000 mL容量瓶配制450 mL 0.1 mol•L-1的鹽酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ②⑥③⑤ | B. | ④⑥③⑤ | C. | ④⑥①③ | D. | ②⑥①⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ,用電子式表示A與B形成的三原子分子的形成過程
,用電子式表示A與B形成的三原子分子的形成過程 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 5.6g的鐵與0.1mol Cl2充分反應轉移電子0.3NA | |
| B. | 一定條件下,2.3g的Na完全與O2反應生成3.6g產物時失去的電子數為0.1NA | |
| C. | 1.0L的0.1 mol•L-1AlCl3溶液中含有的Al3+離子數為0.1NA | |
| D. | 標準狀況下,22.4L的CCl4中含有的CCl4分子數為NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com