
 在25℃,101KPa的條件下,將共8L的CO和O2的混合氣體通入一個帶可自由移動活塞容積可變但壓強不變的密閉容器中(如圖所示),用電火花點燃充分反應后恢復至原來的條件,測得氣體的密度變為原來的$\frac{4}{3}$,求
在25℃,101KPa的條件下,將共8L的CO和O2的混合氣體通入一個帶可自由移動活塞容積可變但壓強不變的密閉容器中(如圖所示),用電火花點燃充分反應后恢復至原來的條件,測得氣體的密度變為原來的$\frac{4}{3}$,求分析 (1)發生反應:2CO+O2$\frac{\underline{\;電火花\;}}{\;}$2CO2,混合氣體總質量不變,充分反應后恢復至原來的條件,測得氣體的密度變為原來的$\frac{4}{3}$,則反應后的體積為原來的$\frac{3}{4}$,即反應后的體積為8L×$\frac{3}{4}$=6L,利用差量法計算參加反應CO、O2的體積,再討論計算原混合氣體中CO和O2可能的體積比;
(2)若反應后氣體的密度在相同條件下為氦氣密度的$\frac{29}{3}$倍,則反應后氣體的相對分子質量為4×$\frac{29}{3}$,反應后氣體為CO2 、O2或CO2 、CO,再計算平均相對分子質量進行驗證解答.
解答 解:(1)混合氣體總質量不變,充分反應后恢復至原來的條件,測得氣體的密度變為原來的$\frac{4}{3}$,則反應后的體積為原來的$\frac{3}{4}$,即反應后的體積為8L×$\frac{3}{4}$=6L,
2CO+O2$\frac{\underline{\;電火花\;}}{\;}$2CO2 體積減小
2 1 2 1
4L 2L 4L 8L-6L=2L
若CO有剩余,則O2為2L,CO為8L-2L=6L,CO和O2的體積比為6L:2L=3:1;
若O2有剩余,則CO為4L,O2為8L-4L=4L,CO和O2的體積比為4L:4L=1:1,
故答案為:3:1;1:1;
(2)若反應后氣體的密度在相同條件下為氦氣密度的$\frac{29}{3}$倍,則反應后氣體的相對分子質量為4×$\frac{29}{3}$,
由(1)計算可知,若反應后為CO2 、O2混合氣體,二者物質的量之比為4L:(4L-2L)=2:1,平均相對分子質量為$\frac{44×2+32}{2+1}$=40,不符合,
若反應后為CO2 、CO混合氣體,二者物質的量之比為4L:(6L-4L)=2:1,平均相對分子質量為$\frac{44×2+28}{3}$=4×$\frac{29}{3}$,符合,
故反應后氣體的成分為CO2 、CO,二者物質的量之比為2:1,
故答案為:CO2 、CO;2:1.
點評 本題考查阿伏伽德羅定律及其推論、混合物有關計算,題目還涉及討論型過量計算,側重考查學生分析計算能力,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | $\frac{20×1{0}^{-3}}{127}$mol | B. | 20M mol | C. | $\frac{20×1{0}^{-3}}{M}$mol | D. | $\frac{20}{M}$mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 鍵,其核磁共振氫譜圖顯示有三重峰,峰面積之比為3:2:3,該有機物不含有CH3-O-,則A的結構簡式為CH3COOCH2CH3.
鍵,其核磁共振氫譜圖顯示有三重峰,峰面積之比為3:2:3,該有機物不含有CH3-O-,則A的結構簡式為CH3COOCH2CH3. 是常用香精,廣泛用于食品、化妝品等行業,可從自然界中提取,也可人工合成.實驗室現以食品防腐劑[主要成分為苯甲酸鈉(
是常用香精,廣泛用于食品、化妝品等行業,可從自然界中提取,也可人工合成.實驗室現以食品防腐劑[主要成分為苯甲酸鈉( )]、甲醇為原料制備苯甲酸甲酯.已知:
)]、甲醇為原料制備苯甲酸甲酯.已知:| 熔點℃ | 沸點℃ | 水溶性 | |
| 甲醇 | -97.8 | 64.7 | 易溶 |
| 苯甲酸 (一元弱酸) | 122.4 | 249.3 | 常溫:0.17g 100℃:6.8g |
| 苯甲酸甲酯 | -12.3 | 198 | 難溶 |


 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 組分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
| 質量分數 | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.16 |

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
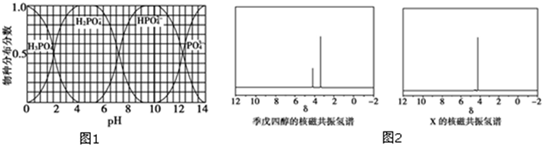
 )與季戊四醇(
)與季戊四醇( )以物質的量之比2:1 反應
)以物質的量之比2:1 反應 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 鐵、銅及其化合物在日常生產、生活有著廣泛的應用.請回答下列問題:
鐵、銅及其化合物在日常生產、生活有著廣泛的應用.請回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com