
| A. | 為防止電池中的重金屬污染土壤和水體,應積極開發廢舊電池的綜合回收利用 | |
| B. | 氫能是清潔能源,工業上電解水法制大量氫氣符合節能減排理念 | |
| C. | 大量的汽車尾氣是造成霧霾天氣的一個重要因素 | |
| D. | 煤的液化和氣化均屬于化學變化 |
分析 A、電池中的重金屬離子會帶來污染;
B、電解水消耗大量的能源;
C、汽車尾氣中含SO2等氣體和顆粒物;
D、沒有新物質生成的變化是物理變化,有新物質生成的變化是化學變化.
解答 解:A、電池中的重金屬離子會帶來污染,為防止電池中的重金屬離子污染土壤和水源,應積極開發廢舊電池的綜合利用技術,故A正確;
B、氫能是清潔能源,但電解水消耗大量的能源,電解水法制大量氫氣不符合節能減排理念,故B錯誤;
C、汽車尾氣釋放出SO2等氣體和顆粒物,是造成霧霾天氣的重要因素之一,故C正確;
D、煤的氣化是將其轉化為可燃性氣體的過程,屬于化學變化;煤的液化是使煤與氫氣作用生成液體燃料,屬于化學變化,故D正確;
故選B.
點評 本題考查原電池對環境的污染、物理變化和霧霾的形成,明確物質的成分和性質即可解答,難度不大.


 口算題卡加應用題集訓系列答案
口算題卡加應用題集訓系列答案 綜合自測系列答案
綜合自測系列答案科目:高中化學 來源:2016-2017學年甘肅省高二上10月月考化學試卷(解析版) 題型:選擇題
下列鹽的水溶液,其pH值小于7的是 ( )
A.NaHCO3溶液 B.NaCl溶液 C.Na2SO4溶液 D.NH4Cl溶液
查看答案和解析>>
科目:高中化學 來源:2017屆重慶一中高三上學期第二次月考化學試卷(解析版) 題型:選擇題
某羧酸酯的分子式為C57H104O6,1 mol該酯完全水解可得到3 mol羧酸M和1 mol甘油[HOCH2CH(OH)CH2OH]。羧酸M的分子式為( )
A.C17H32O2 B.C18H34O2 C.C18H36O2 D.C19H36O2
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
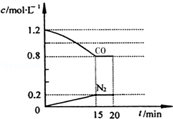 回答下列問題:
回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 向容積固定的容器甲和帶有活塞的定壓容器乙中分別通入2mol SO2和1mol O2(如下圖),若開始通氣時兩容器的體積相同,在相同溫度下反應,一段時間后,反應達到平衡.則下列說法正確的是( )
向容積固定的容器甲和帶有活塞的定壓容器乙中分別通入2mol SO2和1mol O2(如下圖),若開始通氣時兩容器的體積相同,在相同溫度下反應,一段時間后,反應達到平衡.則下列說法正確的是( )| A. | 平衡時,兩容器內SO3的濃度必定相等 | |
| B. | 平衡時,混合氣體中的SO3的體積分數甲比乙高 | |
| C. | SO2的轉化率乙容器內比甲容器內高 | |
| D. | 反應后的相同時間內,甲容器中的反應速率大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向鹽酸中滴加氨水:H++OH-═H2O | |
| B. | 氯化鈣與碳酸氫鉀溶液混合:Ca2++CO32-═CaCO3↓ | |
| C. | 氫氧化鋁中和胃酸:Al(OH)3+3H+═Al3++3H2O | |
| D. | Ca(HCO3)2溶液中加入過量KOH溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 4NH3+5O2═4NO+6H2O | B. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||
| C. | 2NaHCO3═Na2CO3+H2O+CO2 | D. | Cl2+2NaBr═2NaCl+Br2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com