
分析 CH3COOH是弱電解質,部分電離生成CH3COO-、H+;
(1)加入冰醋酸,醋酸濃度增大平衡向正反應方向移動;
(2)濃度越小其電離程度越大;但其電離增大程度小于溶液體積增大程度;
(3)HCl電離出的氫離子抑制醋酸電離;
(4)加入氯化鈉溶液相當于稀釋醋酸,促進醋酸電離.
解答 解:CH3COOH是弱電解質,部分電離生成CH3COO-、H+,電離方程式為CH3COOH?CH3COO-+H+,
故答案為:CH3COOH?CH3COO-+H+;
(1)加入冰醋酸,醋酸濃度增大平衡向正反應方向移動,導致溶液中c(H+)增大,
故答案為:向電離方向移動;增大;
(2)濃度越小其電離程度越大,所以加水稀釋促進醋酸電離,平衡向電離方向移動;但其電離增大程度小于溶液體積增大程度,導致溶液中c(H+)減小,
故答案為:向電離方向移動;減小;
(3)HCl電離出的氫離子抑制醋酸電離,所以抑制醋酸電離,則醋酸向離子結合成分子的方向移動,但溶液中c(H+)增大,
故答案為:向離子結合成分子的方向移動;增大;
(4)加入氯化鈉溶液相當于稀釋醋酸,促進醋酸電離,則醋酸向電離方向移動,因為醋酸電離增大程度小于溶液體積增大程度,所以c(H+)減小,
故答案為:向電離方向移動;減小.
點評 本題考查弱電解質的電離,為高頻考點,明確弱電解質電離特點及電離影響因素是解本題關鍵,知道弱電解質電離程度與其濃度關系,題目難度不大.


 名師點撥卷系列答案
名師點撥卷系列答案 英才計劃期末調研系列答案
英才計劃期末調研系列答案科目:高中化學 來源: 題型:選擇題
| A. | 為防止電池中的重金屬污染土壤和水體,應積極開發廢舊電池的綜合回收利用 | |
| B. | 氫能是清潔能源,工業上電解水法制大量氫氣符合節能減排理念 | |
| C. | 大量的汽車尾氣是造成霧霾天氣的一個重要因素 | |
| D. | 煤的液化和氣化均屬于化學變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 +3HNO3 $→_{△}^{濃硫酸}$
+3HNO3 $→_{△}^{濃硫酸}$ +3H2O;
+3H2O; 查看答案和解析>>
科目:高中化學 來源: 題型:解答題
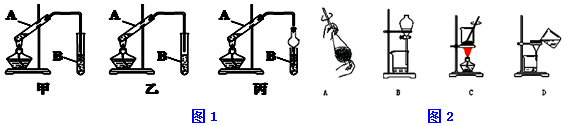
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該氖原子的相對原子質量是12$\frac{a}{b}$ | B. | 該氖原子的摩爾質量是aNAg | ||
| C. | Wg該氖原子的物質的量是$\frac{W}{{a{N_A}}}$mol | D. | Wg該氖原子所含質子數是10W/a |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鐵粉與稀硫酸反應:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 用小蘇打 (NaHCO3)治療胃酸過多:HCO3-+H+═H2O+CO2↑ | |
| C. | 往碳酸鎂中滴加稀鹽酸:CO32-+2H+═H2O+CO2↑ | |
| D. | 氫氧化鋇溶液與稀H2SO4反應:Ba2++SO42-+H++OH-═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
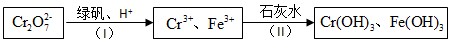
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com