
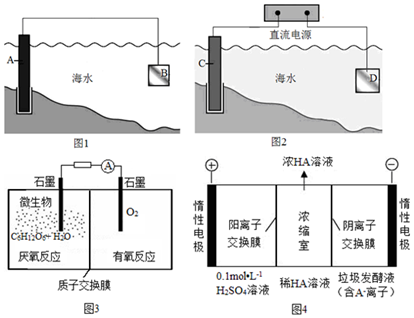
分析 (1)形成原電池時,Fe作正極被保護;活潑性比Fe強的金屬作負極,被腐蝕;Fe作陰極被保護;陽極上氯離子失電子生成氯氣,檢驗氯氣用濕潤的淀粉碘化鉀試紙;
(2)根據圖知,負極上C6H12O6失電子,正極上O2得電子和H+反應生成水,負極的電極反應式為C6H12O6+6H2O-24e-=6CO2+24H+,正極的電極反應式為O2+4e-+4H+═2H2O;
(3)①電解池中陽極上氫氧根離子失電子生成氧氣;
②根據電解池中離子移動方向來回答判斷.
解答 解:(1)形成原電池時,Fe作正極被保護,則要選擇活潑性比Fe強的金屬作負極,所以選鋅;Fe作陰極被保護,則鋼閘門C做陰極;電解氯化鈉溶液時陽極上氯離子失電子生成氯氣,其電極反應為:2Cl--2e-═Cl2↑,檢驗氯氣用濕潤的淀粉碘化鉀試紙,即用濕潤的淀粉碘化鉀試紙放在陽極附近,試紙變藍,證明生成氯氣;故答案為:a;陰;2Cl--2e-═Cl2↑;濕潤的淀粉碘化鉀試紙放在陽極附近,試紙變藍,證明生成氯氣;
(2)根據圖知,負極上C6H12O6失電子,正極上O2得電子和H+反應生成水,負極的電極反應式為C6H12O6+6H2O-24e-=6CO2+24H+,正極的電極反應式為O2+4e-+4H+═2H2O,故答案為:O2+4e-+4H+═2H2O;
(3)①陽極上是陰離子氫氧根離子發生失電子的氧化反應,電極反應式為:4OH--4e-═2H2O+O2↑,故答案為:4OH--4e-═2H2O+O2↑;
②在電解池的陽極上是OH-放電,所以c(H+)增大,并且H+從陽極通過陽離子交換膜進入濃縮室;根據電解原理,電解池中的陰離子移向陽極,即A-通過陰離子交換膜從陰極進入濃縮室,這樣:H++A-═HA,乳酸濃度增大,
故答案為:陽極OH-放電,c(H+)增大,H+從陽極通過陽離子交換膜進入濃縮室,A-通過陰離子交換膜從陰極進入濃縮室,H++A-═HA,乳酸濃度增大.
點評 本題涉及電解池和原電池的工作原理以及應用的考查,注意知識的遷移和應用是解題的關鍵,注意把握原電池和電解池中離子的移動方向,掌握基礎是關鍵,題目難度中等.


科目:高中化學 來源: 題型:選擇題
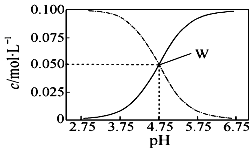 25℃,有c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的一組醋酸和醋酸鈉混合溶液,溶液中c(CH3COOH)、c(CH3COO-)與pH值的關系如圖所示.下列有關離子濃度關系敘述正確的是( )
25℃,有c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的一組醋酸和醋酸鈉混合溶液,溶液中c(CH3COOH)、c(CH3COO-)與pH值的關系如圖所示.下列有關離子濃度關系敘述正確的是( )| A. | pH=5.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | pH=3.5溶液中:c(Na+)+c(H+)+c(OH-)+c(CH3COOH)=0.1mol•L-1 | |
| C. | 該溫度下醋酸的電離平衡常數為10-4.75 | |
| D. | 向W點所表示溶液中加入等體積的0.05 mol•L-1NaOH溶液:c(H+)=c(CH3COOH)+c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金屬的電化腐蝕比化學腐蝕普遍 | B. | 鋼鐵在干燥空氣里不易腐蝕 | ||
| C. | 用鋁質鉚釘接鐵板,鐵板易被腐蝕 | D. | 原電池電路中電子由負極流入正極 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 熱穩定性:Na2CO3>NaHCO3 | |
| B. | 相同溫度時的水溶性:Na2CO3<NaHCO3 | |
| C. | 等物質的量濃度的溶液的堿性:Na2CO3<NaHCO3 | |
| D. | 與同濃度的鹽酸反應的劇烈程度:Na2CO3>NaHCO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鐵與FeCl3溶液反應:Fe+Fe3+═2Fe2+ | |
| B. | Fe與鹽酸反應:2Fe+6H+═2Fe3++3H2↑ | |
| C. | FeCl2溶液與Cl2反應:Fe2++Cl2═Fe3++2Cl- | |
| D. | Fe(OH)3與鹽酸反應:Fe(OH)3+3H+═Fe3++3H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 二氧化硅與氧化鈣(高溫) | B. | 二氧化硅與氫氧化鈉(常溫) | ||
| C. | 二氧化硅與碳(高溫) | D. | 二氧化硅與濃HNO3(常溫) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
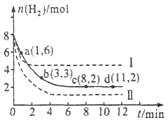 工業上有一種用CO2來生產甲醇燃料的方法:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1
工業上有一種用CO2來生產甲醇燃料的方法:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com