
| c(Br-) |
| c(Cl-) |
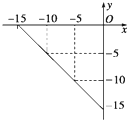
| Ksp(AgBr) |
| Ksp(AgCl) |
| 5.4×10-13 |
| 2×10-10 |
| 10-15 |
| 10-15 |
| 0.01 |


科目:高中化學 來源: 題型:
| A、只有①正確 |
| B、只有③ |
| C、只有①和④ |
| D、①②③④都正確 |
查看答案和解析>>
科目:高中化學 來源: 題型:
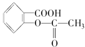 ,作為一種解熱鎮痛藥,對于感冒發燒,它有較好的療效,但大劑量長期空腹服用,容易對胃腸道產生刺激,原因是阿司匹林在胃中會發生酯的水解反應,生成(用結構簡式表示)
,作為一種解熱鎮痛藥,對于感冒發燒,它有較好的療效,但大劑量長期空腹服用,容易對胃腸道產生刺激,原因是阿司匹林在胃中會發生酯的水解反應,生成(用結構簡式表示)查看答案和解析>>
科目:高中化學 來源: 題型:
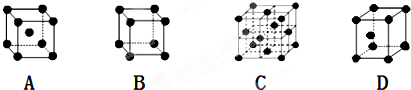
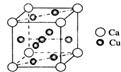 是金屬Ca和Cu所形成的某種合金的晶胞結構示意圖,則該合金中Ca和Cu的原子個數比為
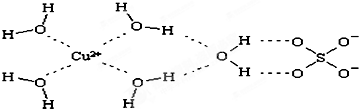
是金屬Ca和Cu所形成的某種合金的晶胞結構示意圖,則該合金中Ca和Cu的原子個數比為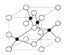 是銅的某種氧化物的晶胞結構示意圖,該晶體的密度為a g/cm3,設阿伏伽德羅常數的值為NA,則該晶胞的體積為
是銅的某種氧化物的晶胞結構示意圖,該晶體的密度為a g/cm3,設阿伏伽德羅常數的值為NA,則該晶胞的體積為查看答案和解析>>
科目:高中化學 來源: 題型:
| 化學鍵 | C-H | C-F | H-F | F-F |
| 鍵能 | 414 | 489 | 565 | 158 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
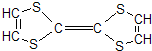 用于制造隱形飛機的某種物質具有吸收微波的功能,其主要成分的結構如圖所示.關于其性質的描述不正確的是( )
用于制造隱形飛機的某種物質具有吸收微波的功能,其主要成分的結構如圖所示.關于其性質的描述不正確的是( )| A、能使溴水和酸性KMnO4溶液褪色 |
| B、1mol該物質可與3molH2完全加成 |
| C、該物質在空氣燃燒產生刺激性氣體 |
| D、該物質屬于烯烴 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com