
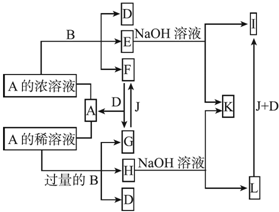
分析 E、H與氫氧化鈉溶液反應分別生成I、L,I和L又能和J、D發生轉化,說明金屬B為變價金屬,B可能為Fe.E、H均為B鹽溶液,A能與B反應生成多種物質,說明A為酸,A與Fe反應時與酸的濃度有關,則A可能是硫酸或硝酸,根據G+J→F可以判斷A是硝酸不是硫酸(氫氣與二氧化硫無法轉化),故酸A為HNO3,B為Fe,結合轉化關系,可推知F為NO2,A為HNO3,E為Fe(NO3)3、D為H2O、I為Fe(OH)3、G為NO、F為O2、H為Fe(NO3)2,L為Fe(OH)2,K為NaNO3,據此解答.
解答 解:E、H與氫氧化鈉溶液反應分別生成I、L,I和L又能和J、D發生轉化,說明金屬B為變價金屬,B可能為Fe.E、H均為B鹽溶液,A能與B反應生成多種物質,說明A為酸,A與Fe反應時與酸的濃度有關,則A可能是硫酸或硝酸,根據G+J→F可以判斷A是硝酸不是硫酸(氫氣與二氧化硫無法轉化),故酸A為HNO3,B為Fe,結合轉化關系,可推知F為NO2,A為HNO3,E為Fe(NO3)3、D為H2O、I為Fe(OH)3、G為NO、F為O2、H為Fe(NO3)2,L為Fe(OH)2,K為NaNO3.
(1)金屬B為Fe,在元素周期表中的位置是:第四周期Ⅷ族,Fe和濃硝酸反應的條件是:加熱,少量Fe與稀硝酸反應的離子方程式:Fe+4H++NO3-=Fe2++NO↑+2H2O,
故答案為:第四周期Ⅷ族;加熱;Fe+4H++NO3-=Fe2++NO↑+2H2O;
(2)常溫下0.1 mol/L Fe(NO3)3的水溶液中Fe3+水解,溶液呈酸性,各離子濃度大小關系為:,
故答案為:c(NO3-)>c(Fe3+)>c(OH-)>c(H+),
故答案為:c(NO3-)>c(Fe3+)>c(OH-)>c(H+);
(3)L轉化成I的現象是:白色沉淀變成灰綠色,最終變成紅褐色,有關的化學方程式:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案為:白色沉淀變成灰綠色,最終變成紅褐色;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(4)檢測Fe(NO3)2溶液中陽離子的存在:取少量H溶液于試管中,先加入幾滴KSN溶液,無明顯現象,再加幾滴新制的氯水,溶液變為血紅色,證明溶液中含有Fe2+,
故答案為:取少量H溶液于試管中,先加入幾滴KSN溶液,無明顯現象,再加幾滴新制的氯水,溶液變為血紅色,證明溶液中含有Fe2+;
(5)等體積混合的瞬間,體積加倍濃度減半,混合后溶液中的c(Fe3+)=2×10-8mol/L,c(OH-)=1×10-8mol/L,則Qc=c(Fe3+)×c3(OH-)=2.0×10-32>Ksp,有沉淀生成,
故答案為:混合后溶液中的c(Fe3+)=2×10-8mol/L,c(OH-)=1×10-8mol/L,則Qc=c(Fe3+)×c3(OH-)=2.0×10-32>Ksp,有沉淀生成.
點評 本題考查無機物推斷,涉及Fe、N元素化合物性質與轉化,需要學生熟練掌握元素化合物性質,側重考查學生分析推理能力,難度較大.


 新題型全程檢測期末沖刺100分系列答案
新題型全程檢測期末沖刺100分系列答案科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分別加入碘水,觀察顏色反應 | |
| B. | 分別加稀硫酸煮沸,再加足量NaOH溶液調至堿性,加銀氨溶液加熱觀察有無銀鏡 | |
| C. | 分別加熱水溶解,觀察溶解性 | |
| D. | 放在嘴里咀嚼,有無甜味產生 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用A濃度表示該反應速率為1.6 mol/(L•min) | |
| B. | 若使容器體積變為1 L,則B的物質的量一定減小 | |
| C. | 達到平衡,測得放出熱量為x kJ,則x=Q | |
| D. | 若向容器再充入1 mol C,重新達到平衡,A的體積分數保持不變,則B為氣態 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 高級脂肪酸甘油酯是高分子化合物 | |
| B. | 天然的不飽和高級脂肪酸甘油酯都是混甘油酯 | |
| C. | 植物油可以使酸性高錳酸鉀溶液褪色 | |
| D. | 油脂皂化完全后原有的液體分層現象消失 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
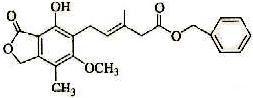
| A. | 一定條件下,既可以與Br2發生加成反應,又可以與Br2發生取代反應 | |
| B. | 1 mol該化合物最多可以與3 molNaOH反應 | |
| C. | 既可以催化加氫,又可以在稀硫酸存在下水解得2種有機物 | |
| D. | 可以與Na2CO3溶液反應放出CO2氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com