
| A. | 工業上用電解熔融的氯化物的方法制備金屬鎂和鋁 | |
| B. | 適當提高合成氨原料氣中N2的含量,可提高H2的轉化率 | |
| C. | 從安全運輸上看,硫酸廠靠近硫酸消費中心比靠近原料產地更為有利 | |
| D. | 利用反應NaCl(飽和)+CO2+NH3+H2O=NH4Cl+NaHCO3↓制取NaHCO3時,應在NaCl飽和溶液中先通入過量CO2再通入過量的NH3 | |
| E. | 硫酸廠生產時常采有高壓條件提高SO2的轉化率 |
分析 A、因為氯化鋁是共價化合物,所以熔融時,它是不導電的,所以只能去電解氧化鋁;
B、增大一種反應物濃度使平衡向正反應方向移動,提高另一種物質的轉化率;
C、從安全運輸上看,硫酸廠靠近硫酸消費中心比靠近原料產地更為有利;
D、由于二氧化碳溶度積較小,應在NaCl飽和溶液中先通入的NH3再通入過量的過量CO2;
E、由于常壓下三氧化硫的體積分數已達91%,若再加壓對設備及電力系統要求高、成本高,使生產效益低.
解答 解:A、氯化鋁是共價化合物,所以熔融時,它是不導電的,所以只能去電解氧化鋁,故A錯誤
B、增大一種反應物濃度使平衡向正反應方向移動,提高另一種物質的轉化率,所以適當提高合成氨原料氣中N2的含量,使平衡向正反應方向移動,可提高H2的轉化率,故B正確;
C、從安全運輸上看,硫酸廠靠近硫酸消費中心比靠近原料產地更為有利,故C正確;
D、由于二氧化碳溶度積較小,應在NaCl飽和溶液中先通入的NH3再通入過量的過量CO2,故D錯誤;
E、常壓下三氧化硫的體積分數已達91%,二氧化硫轉化率已經很高,若再加壓對設備及電力系統要求高、成本高,使生產效益低,故E錯誤;
故答案為:ADE.
點評 本題考查化學與工業生產,注意化學在工業生成中的應用知識是現在考試的熱點,可以根據教材知識來回答,難度不大.


 小學教材全測系列答案
小學教材全測系列答案 小學數學口算題卡脫口而出系列答案
小學數學口算題卡脫口而出系列答案 優秀生應用題卡口算天天練系列答案
優秀生應用題卡口算天天練系列答案 浙江之星課時優化作業系列答案
浙江之星課時優化作業系列答案科目:高中化學 來源: 題型:解答題
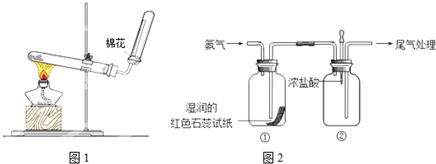
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 增大壓強,反應速率減小 | |
| B. | 最終可生成0.2 mol NH3 | |
| C. | 升髙溫度,反應速率增大 | |
| D. | 當V正(N2):V 正(H2)=1:3時,一定達化學平衡狀態 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
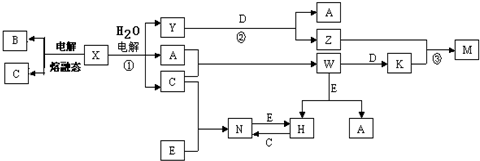
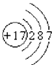 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
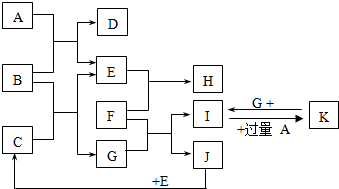 如圖為一些常見物質間的相互轉化關系,其中F為金屬,高溫下能與某些金屬氧化物反應,是工業冶煉金屬的方法之一. A為無色氣體,B為淡黃色固體,C為無色液體,E和J為無色氣體單質.
如圖為一些常見物質間的相互轉化關系,其中F為金屬,高溫下能與某些金屬氧化物反應,是工業冶煉金屬的方法之一. A為無色氣體,B為淡黃色固體,C為無色液體,E和J為無色氣體單質.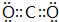 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用25 mL量筒量取12.36 mL鹽酸 | B. | 托盤天平稱取8.75克食鹽 | ||
| C. | 用酸式滴定管量取4.90mL硫酸 | D. | 用廣泛pH試紙測得某溶液pH為3.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用鐵作陽極,電解飽和食鹽水的離子方程式:Fe+2H2O$\frac{\underline{\;電解\;}}{\;}$Fe(OH)2↓+H2↑ | |
| B. | 溴乙烷的消去反應:CH3CH2Br$→_{△}^{濃硫酸}$ CH2=CH2↑+HBr | |
| C. | CH4燃燒熱的熱化學方程式:CH4(g)+2O2(g)═CO2(g)+2H2O(g) H=-802.3 kJ•mol-1 | |
| D. | 示蹤原子法研究乙酸與乙醇酯化反應: |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com