
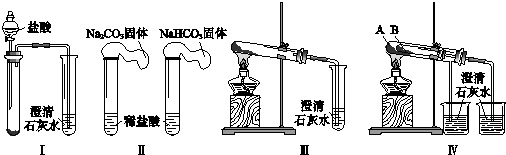
分析 (1)稀鹽酸足量說明兩種固體完全反應,質量相同含碳量越高,完全反應生成二氧化碳的量越多;
(2)碳酸氫鈉在加熱條件下能分解生成碳酸鈉和水、二氧化碳;根據兩個實驗的區別分析;
(3)根據碳酸氫鈉的性質分析.
解答 解:(1)稀鹽酸足量說明兩種固體完全反應,質量相同含碳量越高,完全反應生成二氧化碳的量越多,碳酸鈉中含碳量為$\frac{12}{106}$=11.3%,而碳酸氫鈉中含碳量為$\frac{12}{84}$=14.3%,所以碳酸鈉放出二氧化碳量少,故答案為:Na2CO3;
(2)碳酸氫鈉在加熱條件下能分解生成碳酸鈉和水、二氧化碳2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;CO2+Ca(OH)2═CaCO3↓+H2O;實驗Ⅲ、Ⅳ相比,IV可以做到一套裝置同時進行兩個對比實驗,而III不能,故選c,故答案為:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,CO2+Ca(OH)2═CaCO3↓+H2O;c;
(3)碳酸鈉直接加熱不產生氣體,而碳酸氫鈉不直接加熱就產生氣體,就更說明碳酸氫鈉不穩定,所以試管B中裝入的固體最好是碳酸氫鈉.
故答案為:NaHCO3.
點評 本題考查了碳酸鈉和碳酸氫鈉的性質,難度不大,明確碳酸鈉和鹽酸反應分兩步進行.


科目:高中化學 來源: 題型:選擇題
| A. | 2CO(g)+O2(g)═2CO2(g)△H=-141.3kJ•mol-1 | |
| B. | CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-141.3kJ•mol-1 | |
| C. | CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-282.6kJ•mol-1 | |
| D. | CO(g)+O2(g)═CO2(g)△H=-141.3kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 28 g氮氣所含有的原子數目為NA | |
| B. | 在常溫常壓下,11.2 L N2含有的分子數為0.5 NA | |
| C. | 0.5 mol單質鐵與足量鹽酸反應轉移電子數為NA | |
| D. | 標準狀況下,1 L水所含分子數為$\frac{1}{22.4}$NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 高純度的硅廣泛用于制作光導纖維,光導纖維遇強堿會“斷路” | |
| B. | 煤經過氣化和液化兩個物理變化,可變為清潔能源 | |
| C. | 如將材料均勻分散到某液體分散劑中,該分散系可發生丁達爾現象,由此可推測該材料的直徑為1~100pm之間 | |
| D. | 屠呦呦女士利用乙醚萃取青蒿素獲得了2015年度諾貝爾生理學或醫學獎,為人類防治瘧疾作出了重大貢獻 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 所有自發進行的化學反應都是放熱反應 | |
| B. | 高溫高壓下可以使石墨轉化為金剛石是自發的化學反應 | |
| C. | 由能量判據和熵判據組合而成的復合判據,將更適合于所有的過程 | |
| D. | 同一物質的固、液、氣三種狀態的熵值相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | O→a時的反應的離子方程式為:Ba2++2OH-+SO42-+2H+═BaSO4↓+2 H2O | |
| B. | a→b時發生的離子反應為H++OH-═H2O | |
| C. | 原混合溶液中 C(HCl):C(MgSO4)=3:1 | |
| D. | 從a→b→c說明溶液中結合OH-的能力強弱為:H+>Mg2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com