
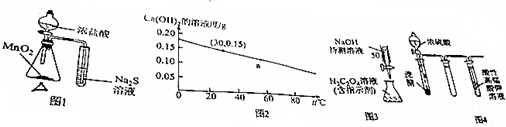
| A. | 圖1的裝置可用于比較MnO2、Cl2、S的氧化性 | |
| B. | 圖2可知:30℃時Ca(OH)2溶液的濃度一定大于60℃時的溫度 | |
| C. | 圖3的裝置可用于已知濃度的H2C2O4溶液測定未知濃度的NaOH溶液 | |
| D. | 圖4的實驗現象:酸性高錳酸鉀溶液中有氣泡出現,且溶液顏色逐漸變淺乃至褪去 |
分析 A.同一氧化還原反應中,氧化劑的氧化性大于氧化產物的氧化性;
B.根據圖知,30℃時Ca(OH)2溶液的溶解度一定大于60℃時的溫度,但30℃時Ca(OH)2溶液的濃度不一定大于60℃時的溫度;
C.酸式滴定管只能盛放酸性溶液,堿性溶液應該用堿式滴定管盛放;
D.乙醇被高錳酸鉀溶液氧化生成乙酸.
解答 解:A.該實驗中,加熱條件下,濃鹽酸和二氧化錳反應生成氯氣,氯氣具有強氧化性,能氧化硫化鈉生成硫單質,濃鹽酸和二氧化錳的反應中二氧化錳是氧化劑、氯氣是氧化物,所以氧化性:二氧化錳大于氯氣;氯氣和硫化鈉的反應中,氯氣是氧化劑、S是氧化產物,則氧化性氯氣大于S,由此得出氧化性MnO2>Cl2>S,故A正確;
B.根據圖知,30℃時Ca(OH)2溶液的溶解度一定大于60℃時的溫度,但30℃時Ca(OH)2溶液的濃度不一定大于60℃時的溫度,可能相等也可能小于,故B錯誤;
C.酸式滴定管只能盛放酸性溶液,堿性溶液應該用堿式滴定管盛放,NaOH溶液應該用堿式滴定管盛放,故C錯誤;
D.乙醇能被高錳酸鉀溶液氧化生成乙酸而使酸性高錳酸鉀溶液褪色,所以酸性高錳酸鉀溶液褪色但沒有氣體生成,故D錯誤;
故選A.
點評 本題考查化學實驗方案評價,為高頻考點,涉及氧化性強弱比較、溶解度與濃度關系、儀器的選取、乙醇的性質等知識點,側重考查學生分析判斷及基本操作能力,明確實驗原理及基本操作方法是解本題關鍵,注意從實驗操作規范性及評價性分析解答,易錯選項是BD.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
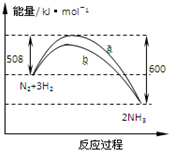
| A. | 1 mo N2與3 mo H2反應可以放出92 kJ的熱量 | |
| B. | b曲線是加入催化劑時的能量變化曲線 | |
| C. | 加入催化劑,該反應的焓變減小 | |
| D. | 正反應的活化能等于逆反應的活化能 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1molCO2的質量為44g/mol | |
| B. | CO2的摩爾質量為44g | |
| C. | CO2的摩爾質量等于CO2的相對分子質量 | |
| D. | NA個CO2的質量與CO2的相對分子質量在數值上相同(NA為阿伏加德羅常數) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ,B
,B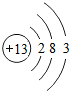 ,二者離子半徑:Na+>Al3+(填離子符號).
,二者離子半徑:Na+>Al3+(填離子符號).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 發生的化學反應是復分解反應 | |
| B. | 反應的生成物中有Na2CO3 | |
| C. | 反應后形成的混合物的聚集顆粒直徑為1~100nm | |
| D. | 反應說明硅酸易溶于水 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
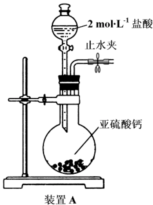


查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 溫度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com