
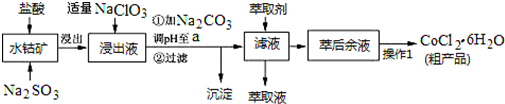
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 開始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
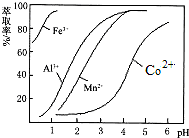
分析 含鈷廢料中加入鹽酸、Na2SO3,加入鹽酸和Na2SO3,可得CoCl2、AlCl3、FeCl2,加入NaClO3,發生氧化還原反應可得到FeCl3,然后加入Na2CO3調pH至5.2,可得到Fe(OH)3、Al(OH)3沉淀,過濾后所得濾液主要含有CoCl2,為得到CoCl2•6H2O晶體,應控制溫度在86℃以下,加熱時要防止溫度過高而失去結晶水,可減壓烘干,
(1)酸性條件下,Co2O3和SO32-發生氧化還原反應生成Co2+、SO42-;
(2)酸性條件下,氯酸根離子能氧化亞鐵離子生成鐵離子,自身被還原生成氯離子;
酸性條件下ClO3-和Cl-發生氧化還原反應生成Cl2;
(3)“加Na2CO3調pH至a”,目的是除去鐵離子、鋁離子,所以需要將鐵離子、鋁離子轉化為沉淀;
(4)CoCl2•6H2O熔點為86℃,加熱至110~120℃時,失去結晶水生成無水氯化鈷;
(5)由表中數據可知,調節溶液PH在3.0~3.5之間,可使Mn2+完全沉淀,并防止Co2+轉化為Co(OH)2沉淀;
(6)根據CoCl2•6H2O的組成分析,可能是含有雜質,也可能是失去部分水.
解答 解:含鈷廢料中加入鹽酸、Na2SO3,加入鹽酸和Na2SO3,可得CoCl2、AlCl3、FeCl2,加入NaClO3,發生氧化還原反應可得到FeCl3,然后加入Na2CO3調pH至5.2,可得到Fe(OH)3、Al(OH)3沉淀,過濾后所得濾液主要含有CoCl2,為得到CoCl2•6H2O晶體,應控制溫度在86℃以下,加熱時要防止溫度過高而失去結晶水,可減壓烘干,
(1)酸性條件下,Co2O3和SO32-發生氧化還原反應生成Co2+、SO42-,離子方程式為Co2O3+SO32-+4H+=2Co2++SO42-+2H2O,
故答案為:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O;
(2)酸性條件下,氯酸根離子能氧化亞鐵離子生成鐵離子,自身被還原生成氯離子,離子方程式為ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;
酸性條件下ClO3-和Cl-發生氧化還原反應生成Cl2,所以可能可能產生有毒氣體氯氣,離子方程式為ClO3-+5Cl-+6H+=3Cl2↑+3H2O,
故答案為:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;ClO3-+5Cl-+6H+=3Cl2↑+3H2O;
(3)“加Na2CO3調pH至a”,目的是除去鐵離子、鋁離子,所以需要將鐵離子、鋁離子轉化為沉淀,碳酸根離子和鋁離子、鐵離子發生雙水解反應生成二氧化碳和氫氧化物沉淀,所以這兩種沉淀的化學式為Fe(OH)3、Al(OH)3,故答案為:Fe(OH)3、Al(OH)3;
(4)CoCl2•6H2O熔點為86℃,加熱至110~120℃時,失去結晶水生成無水氯化鈷,所以制得的CoCl2•6H2O在烘干時需減壓烘干的原因是降低烘干溫度,防止產品分解,故答案為:降低烘干溫度,防止產品分解;
(5)根據流程圖可知,此時溶液中存在Mn2+、Co2+金屬離子;
由萃取劑對金屬離子的萃取率與pH的關系可知,調節溶液pH在3.0~3.5之間,可使Mn2+完全沉淀,并防止Co2+轉化為Co(OH)2沉淀,
故答案為:除去溶液中的Mn2+;B;
(6)根據CoCl2•6H2O的組成分析,造成產品中CoCl2•6H2O的質量分數大于100%的原因可能是:含有雜質,導致氯離子含量大或結晶水化物失去部分水,導致相同質量的固體中氯離子含量變大,
故答案為:粗產品含有可溶性氯化物或晶體失去了部分結晶水.
點評 本題通過制取CoCl2•6H2O的工藝流程考查了物質制備方案的設計,理解工藝流程圖中可能發生的反應、實驗操作與設計目的、相關物質的性質是解答本題的關鍵,試題充分考查了學生的分析、理解能力及靈活應用所學知識的能力,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,7.8gNa2S固體和7.8gNa2O2固體中含有的陰離子數目均為0.1NA | |
| B. | 在標準狀況下,22.4LCl2和HCl的混合氣體中含有的分子總數為2×6.02×1023 | |
| C. | 含1molFeCl3的飽和溶液滴入沸水中得到膠體數目為NA | |
| D. | 標準狀況下,Na2O2與足量的CO2反應生成2.24LO2,轉移電子數為0.4NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
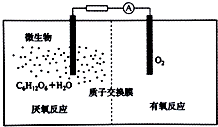 氫氣是一種清潔能源,氫氣的制取與儲存是氫能源利用領域的研究熱點.
氫氣是一種清潔能源,氫氣的制取與儲存是氫能源利用領域的研究熱點.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 最外層有6個電子 | B. | 位于元素周期表的第七周期 | ||
| C. | 主要化合價為-4價、+4價 | D. | “類鉛”不能和鹽酸反應放出氫氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Co2O3 | B. | Co3O3 | C. | Co3O4 | D. | Co5O7 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 若T1=T2,則x1>x2 | B. | 若T1=T2,則x1<x2 | C. | 若T1<T2,則x1=x2 | D. | 若T1<T2,則x1<x2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com