
 氫氣是一種清潔能源,氫氣的制取與儲存是氫能源利用領域的研究熱點.
氫氣是一種清潔能源,氫氣的制取與儲存是氫能源利用領域的研究熱點.分析 (1)利用蓋斯定律解答,從待求反應出發分析反應物、生成物在所給反應中的位置,通過相互加減可得CH4(g)+2H2O(g)═CO2(g)+4H2(g)的熱化學方程式;
(2)依據影響化學反應速率因素分析判斷增大反應速率的試劑,注意原電池反應的分析判斷;
(3)燃料電池電極反應式書寫,用總反應減去一個電極反應式就得另一個電極反應式;
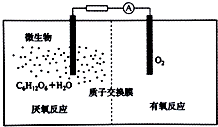
(4)①根據圖知,負極上C6H12O6失電子,正極上O2得電子和H+反應生成水,負極的電極反應式為C6H12O6+6H2O-24e-=6CO2+24H+,正極的電極反應式為O2+4e-+4H+═2H2O;
②該反應屬于燃料電池,燃料電池的電池反應式和燃燒反應式相同.
解答 解:(1)①CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.2kmol-1
②CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=-247.4kJmol-1
據蓋斯定律,①×2-②得:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+659.8kJ•mol-1,
故答案為:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+659.8kJ•mol-1;
(2)若加入少量下列試劑中生成氫氣反應速率增大,則
A.加入濃HNO3 溶液具有強氧化性,和鋅反應不能生成氫氣,故A不符合;
B.加入CH3COONa(固體)溶解后和稀硫酸反應生成醋酸屬于弱酸,反應速率減小,故B不符合;
C.加入Na2SO4固體不影響反應的速率,故C不符合;
D.加入CuSO4 溶液,和鋅反應生成銅,銅和鋅在稀硫酸溶液中形成原電池反應,生成氫氣速率增大,故D符合;
故答案為:D;
(3)這是氫氧燃料電池,負極發生氧化反應,是H2在反應,注意電解質溶液顯堿性,H2得電子不能寫出H+,因為其能和OH-反應,負極反應為H2+2OH--2e-═2H2O;
氫氣燃燒本身無污染,但產生光能等,并且熱能損耗較大,而氫氧燃料電池,是化學能直接轉化為電能,無光能等產生,所以燃料電池的能量轉化率高,
故答案為:H2+2OH--2e-═2H2O;燃料電池的能量轉化率遠高于普通燃燒過程;
(4)①根據圖知,負極上C6H12O6失電子,正極上O2得電子和H+反應生成水,負極的電極反應式為C6H12O6+6H2O-24e-=6CO2+24H+,正極的電極反應式為O2+4e-+4H+═2H2O,因此CO2在負極產生,故答案為:C6H12O6-24e-+6H2O=6 CO2+24H+;
②該反應屬于燃料電池,燃料電池的電池反應式和燃燒反應式相同,則電池反應式為C6H12O6+6O2=6CO2+6H2O,故答案為:C6H12O6+6O2=6CO2+6H2O.
點評 本題考查熱化學方程式書寫、化學電源新型電池,為高頻考點,正確判斷電解質溶液酸堿性是解本題關鍵,所有原電池中都是負極上失電子發生氧化反應、正極上得電子發生還原反應,難點是電極反應式的書寫,主要涉及到蓋斯定律、氧化還原、弱電解質的電離平衡的移動、燃料電池,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 在溫度、壓力一定的條件下,焓因素和熵因素共同決定一個化學反應的方向 | |
| B. | 溫度、壓力一定時,放熱的熵增加反應不一定能自發進行 | |
| C. | 反應焓變是決定反應能否自發進行的唯一因素 | |
| D. | 固體的溶解過程只與焓變有關 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| 選項 | 實驗方案 | 實驗結果 |
| A | 將SO2氣體依次通過NaHCO3溶液、溴水、品紅溶液、澄清石灰水 | 品紅無變化,澄清石灰水變渾濁 |
| B | 將過量二氧化硫氣體通入碳酸氫鈉溶液中,逸出的氣體通入澄清石灰水 | 澄清石灰水變渾濁 |
| C | 取相同體積、相同物質的量濃度的NaHSO3與Na2CO3溶液,分別加入等體積、等濃度的少量鹽酸 | 前者產生氣體體積大于后者的 |
| D | 分別配置SO2和CO2的飽和溶液,立即測定兩種飽和液的pH | 前者的pH小于后者的 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
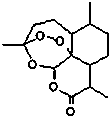 東晉醫藥學家葛洪的《肘后備急方•治寒熱諸瘧方》記載有“青蒿一握,以水二升漬,絞取汁,盡服之”的說法,說明不能加熱青蒿,因高溫可能使活性成分受損.中國藥學家屠呦呦用沸點只有35℃的乙醚作為溶劑來提取青蒿素,創制出新型抗瘧藥青蒿素和雙氫青蒿素,為此獲得2015年諾貝爾生理學或醫學獎.已知青蒿素的結構如圖所示,下列有關青蒿素的說法,不正確的是( )
東晉醫藥學家葛洪的《肘后備急方•治寒熱諸瘧方》記載有“青蒿一握,以水二升漬,絞取汁,盡服之”的說法,說明不能加熱青蒿,因高溫可能使活性成分受損.中國藥學家屠呦呦用沸點只有35℃的乙醚作為溶劑來提取青蒿素,創制出新型抗瘧藥青蒿素和雙氫青蒿素,為此獲得2015年諾貝爾生理學或醫學獎.已知青蒿素的結構如圖所示,下列有關青蒿素的說法,不正確的是( )| A. | 分子式為C15H22O5 | |
| B. | 能夠發生水解反應 | |
| C. | 用沸點只有35℃的乙醚作為溶劑來提取青蒿素的方法化學上叫萃取 | |
| D. | 青蒿素能夠治療瘧疾可能與結構中存在過氧鍵或酯基等基團有關 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 元素代號 | X | Y | Z | W |
| 原子半徑/pm | 160 | 143 | 70 | 66 |
| 主要化合價 | +2 | +3 | +5、+3、-3 | -2 |
| A. | X單質、Y單質工業上均用電解其氧化物法得來 | |
| B. | Z、W兩元素形成的不同化合物,Z的化合價一定不同 | |
| C. | Y的氧化物能與酸反應也能與堿反應,所以既是酸性氧化物又是堿性氧化物 | |
| D. | 一定條件下,W單質可以將Z單質從其氫化物中置換出來 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
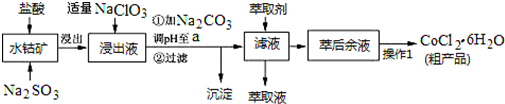
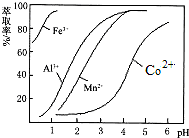
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 開始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .Y2 Z2遇水很易反應,產生的氣體能使品紅溶液褪色,則其與水反應的化學方程式為2S2Cl2+2H2O═SO2↑+3S↓+4HCl
.Y2 Z2遇水很易反應,產生的氣體能使品紅溶液褪色,則其與水反應的化學方程式為2S2Cl2+2H2O═SO2↑+3S↓+4HCl查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com