
| A. | 常溫常壓下,7.8gNa2S固體和7.8gNa2O2固體中含有的陰離子數目均為0.1NA | |
| B. | 在標準狀況下,22.4LCl2和HCl的混合氣體中含有的分子總數為2×6.02×1023 | |
| C. | 含1molFeCl3的飽和溶液滴入沸水中得到膠體數目為NA | |
| D. | 標準狀況下,Na2O2與足量的CO2反應生成2.24LO2,轉移電子數為0.4NA |
分析 A、Na2S和Na2O2的摩爾質量均為78g/mol,且均由2個鈉離子和1個陰離子構成;
B、求出混合氣體的物質的量,然后根據分子個數N=nNA來分析;
C、一個氫氧化鐵膠粒是多個氫氧化鐵的聚集體;
D、求出氧氣的物質的量,然后根據反應過程中氧元素的價態由-1價變為0價來分析.
解答 解:A、Na2S和Na2O2的摩爾質量均為78g/mol,故7.8g混合物的物質的量為0.1mol,而兩者均由2個鈉離子和1個陰離子構成,故0.1mol混合物中含0.1mol陰離子即0.1NA個,故A正確;
B、標況下22.4L氯氣和HCl的物質的量為1mol,故分子個數N=nNA=NA個,故B錯誤;
C、一個氫氧化鐵膠粒是多個氫氧化鐵的聚集體,故1mol氯化鐵所形成的膠粒的個數小于NA個,故C錯誤;
D、標況下2.24L氧氣的物質的量為0.1mol,而反應過程中氧元素的價態由-1價變為0價,故生成0.1mol氧氣時轉移0.2mol電子即0.2NA個,故D錯誤.
故選A.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 在溫度、壓力一定的條件下,焓因素和熵因素共同決定一個化學反應的方向 | |
| B. | 溫度、壓力一定時,放熱的熵增加反應不一定能自發進行 | |
| C. | 反應焓變是決定反應能否自發進行的唯一因素 | |
| D. | 固體的溶解過程只與焓變有關 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 漂白粉變質后的殘留固體有碳酸鈣 | |
| B. | 實驗室可用濃硫酸干燥硫化氫 | |
| C. | 將稀氨水滴到氫氧化鈉溶液中可以制取氨氣 | |
| D. | 單質氯氣及單質硫與鐵反應生成的產物中,鐵的化合價相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 兩份質量相同的鎂分別與足量氮氣、二氧化碳反應,增重的質量相同 | |
| B. | 兩份質量相同的硫分別與足量氫氧化鈉和鈉反應,兩者轉移的電子數相同 | |
| C. | 相同物質的量CO2、H2O分別與足量Na2O2反應,生成氣體的體積相同 | |
| D. | 氫氣分別通過灼熱的CuO和Fe2O3粉末,當轉移電子數相同時,固體減輕的質量相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| 選項 | 實驗方案 | 實驗結果 |
| A | 將SO2氣體依次通過NaHCO3溶液、溴水、品紅溶液、澄清石灰水 | 品紅無變化,澄清石灰水變渾濁 |
| B | 將過量二氧化硫氣體通入碳酸氫鈉溶液中,逸出的氣體通入澄清石灰水 | 澄清石灰水變渾濁 |
| C | 取相同體積、相同物質的量濃度的NaHSO3與Na2CO3溶液,分別加入等體積、等濃度的少量鹽酸 | 前者產生氣體體積大于后者的 |
| D | 分別配置SO2和CO2的飽和溶液,立即測定兩種飽和液的pH | 前者的pH小于后者的 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
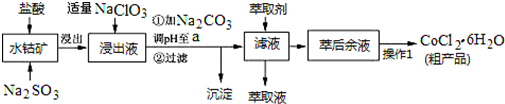
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 開始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
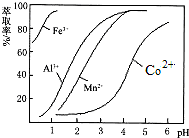
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com