
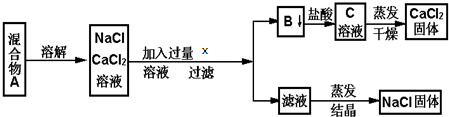
分析 分離NaCl和CaCl2兩種固體混合物,溶解后加入過量碳酸鈉溶液,生成碳酸鈣沉淀和氯化鈉,碳酸鈣和鹽酸發生:CaCO3+2H+=Ca2++CO2↑+H2O,得到氯化鈣溶液,經蒸發可得到氯化鈣固體;
由于碳酸鈉過量,所以濾液中的物質有氯化鈉和碳酸鈉,因此要得到純凈的氯化鈉就需要除去碳酸鈉,加入稀鹽酸最合適,碳酸鈉和稀鹽酸生成氯化鈉和水和二氧化碳,蒸發后最后的固體物質是氯化鈉.
解答 解:(1)分離NaCl和CaCl2兩種固體混合物,溶解后加入過量碳酸鈉溶液,生成碳酸鈣沉淀和氯化鈉,故答案為:Na2CO3;
(2)由于碳酸鈉過量,所以濾液中的物質有氯化鈉和碳酸鈉,因此要得到純凈的氯化鈉就需要除去碳酸鈉,向濾液中加入適量鹽酸至不產生氣體,生成氯化鈉和水和二氧化碳,蒸發后最后的固體物質是氯化鈉,故答案為:加入適量鹽酸至不產生氣體;
(3)要測定該樣品中NaCl和CaCl2的質量比,可稱量干燥的碳酸鈣的質量,根據反應CaCO3+2H+=Ca2++CO2↑+H2O可計算氯化鈣的質量,混合物A的總質量減去氯化鈣的質量可得氯化鈉的質量,故答案為:A.
點評 本題考查物質的分離、提純知識,為高頻考點,側重于學生的分析能力和實驗能力的考查,注意把握實驗的原理和操作方法,為解答該題的關鍵,難度不大.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 氧化產物與還原產物的粒子個數比為5:2 | |
| B. | 氧化產物與還原產物的粒子個數比為2:5 | |
| C. | 氧化劑與還原劑的粒子個數之比為1:8 | |
| D. | 氧化劑與還原劑的粒子個數之比為1:5 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 石油是混合物 | |
| B. | 油脂是天然高分子化合物 | |
| C. | 銅的活動性比鐵弱,可在海輪外殼裝銅塊減緩海輪腐蝕 | |
| D. | 氨氣顯堿性,可用濃硫酸干燥 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4LN2與CO混合氣體的質量為28g | |
| B. | 常溫常壓下,金屬與酸反應生成2g H2,轉移電子數為2NA | |
| C. | 含0.2NA個陰離子的Na2O2和水反應時,轉移0.2mol電子 | |
| D. | 1L1mol•L-1的氨水,含NA個NH3•H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 1種 | B. | 2種 | C. | 3 種 | D. | 4種 |
查看答案和解析>>
科目:高中化學 來源:2017屆江西省高三上學期期中化學試卷(解析版) 題型:選擇題
下列說法或實驗操作正確的是
A. 決定反應速率的主要因素有濃度、壓強、溫度
B. 容量瓶、量筒個滴定管上都標有使用溫度,容量瓶無“0”刻度,量筒、滴定管有“0”刻度;實驗時滴定管水洗后還需潤洗,但容量瓶水洗后不用潤洗
C. 為實驗安全,金屬鈉切割下來的表層物質反應放回原試劑瓶,不能再研磨氯酸鉀或硝酸鉀
D. 皂化反應結束后的混合液中加入飽和食鹽水,再通過分液操作分離出硬質酸鈉
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com