
| A. | 1 641.0 kJ•mol-1 | B. | -1 641.0 kJ•mol-1 | ||
| C. | -259.7 kJ•mol-1 | D. | -519.4 kJ•mol-1 |
分析 ①Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g)△H=489.0kJ•mol-1
②CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0kJ•mol-1
③C(石墨)+O2(g)═CO2 (g)△H=-393.5kJ•mol-1,
由蓋斯定律可知,③×6-②×6-①×2得到4Fe(s)+3O2(g)═2Fe2O3(s),以此計算△H.
解答 解:①Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g)△H=489.0kJ•mol-1
②CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0kJ•mol-1
③C(石墨)+O2(g)═CO2 (g)△H=-393.5kJ•mol-1,
由蓋斯定律可知,③×6-②×6-①×2得到4Fe(s)+3O2(g)═2Fe2O3(s),其△H=(-393.5kJ•mol-1)×6-(-283.0kJ•mol-1)×6-(489.0kJ•mol-1)×2=-1 641.0 kJ•mol-1,
故選B.
點評 本題考查反應熱與焓變,為高頻考點,把握反應中能量變化、已知反應與目標反應的關系為解答的關鍵,側重分析與應用能力的考查,注意蓋斯定律的應用,題目難度不大.


科目:高中化學 來源: 題型:解答題


| 實驗編號 | 試管甲中試劑 | 試管乙中試劑 | 有機層的厚度/cm |
| A | 2 mL乙醇、1 mL乙酸、 1mL18mol•L-1 濃硫酸 | 飽和Na2CO3溶液 | 3.0 |
| B | 2 mL乙醇、1 mL乙酸 | 0.1 | |
| C | 2 mL乙醇、1 mL乙酸、 3 mL 2mol•L-1 H2SO4 | 0.6 | |
| D | 2 mL乙醇、1 mL乙酸、鹽酸 | 0.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 反應①中電能轉化為化學能 | |
| B. | 反應②為放熱反應 | |
| C. | 反應③使用催化劑,△H3減小 | |
| D. | 反應CH4(g)=C(s)+2H2(g)的△H3=74.8kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 任何酸與堿發生中和反應生成1 mol H2O的過程中,能量變化均相同 | |
| B. | 同溫同壓下,H2(g)+Cl2(g)═2HCl(g)在光照和點燃條件下的△H不同 | |
| C. | 化學反應吸收或放出熱量的多少與參加反應的物質的多少無關 | |
| D. | C(石墨,s)═C(金剛石,s)△H>0,所以石墨比金剛石穩定 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
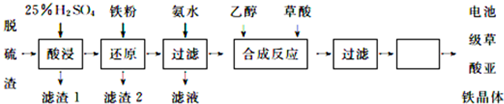
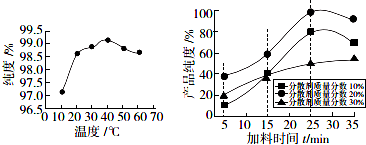
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
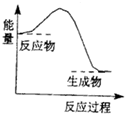
| A. | 生石灰溶于水 | |
| B. | 高溫條件下鋁與氧化鐵的反應 | |
| C. | 高溫條件下碳粉與二氧化碳的反應 | |
| D. | Ba(OH)2•8H2O晶體與NH4C1固體的反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com