
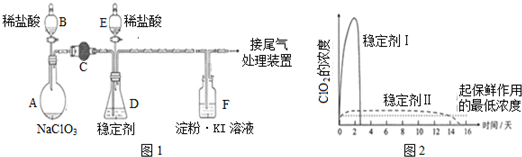
分析 (1)根據儀器特征,可知儀器E是分液漏斗;
(2)A中發生反應是氯酸鈉和鹽酸發生的氧化還原反應生成氯氣、二氧化氯等物質,結合原子守恒書寫化學方程式:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O.為使ClO2在D中被穩定劑充分吸收,產生ClO2的速率要慢;
(3)由圖可知,穩定劑Ⅱ可以緩慢釋放ClO2,能較長時間維持保鮮所需的濃度;
(4)①根據配制一定物質的量濃度的溶液使用的儀器解答;
②根據關系式2ClO2~5I2~10Na2S2O3計算c(ClO2);
③ClO2很不穩定,步驟2所得溶液放置時間太長,相當于消耗的ClO2偏大.
解答 解:(1)根據儀器特征,可知儀器E是分液漏斗,故答案為:分液漏斗;
(2)A中發生反應是氯酸鈉和鹽酸發生的氧化還原反應生成氯氣、二氧化氯等物質,結合原子守恒書寫化學方程式:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O,為使ClO2在D中被穩定劑充分吸收,產生ClO2的速率要慢,故滴加稀鹽酸的速度要慢,
故答案為:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O;慢;
(3)由圖可知,穩定劑Ⅱ可以緩慢釋放ClO2,能較長時間維持保鮮所需的濃度,所以穩定劑Ⅱ好,
故答案為:Ⅱ;穩定劑Ⅱ可以緩慢釋放ClO2,能較長時間維持保鮮所需的濃度;
(4)①配制100mL溶液用到的儀器有托盤天平、藥匙、玻璃棒、膠頭滴管、燒杯、100mL容量瓶、量筒(可用可不用),故還需要的玻璃儀器有:100mL容量瓶、膠頭滴管,
故答案為:100mL容量瓶;膠頭滴管;
②設原ClO2溶液的濃度為x,
2ClO2~5I2~10Na2S2O3
2mol 10mol
$\frac{1{0}^{-2}x×{{V}_{1}}^{-3}}{1{0}^{-1}}$ 1×10-3cV2mol
x=$\frac{2c{V}_{2}}{{V}_{1}}$mol/L=$\frac{135c{V}_{2}}{{V}_{1}}$g/L,
故答案為:$\frac{135c{V}_{2}}{{V}_{1}}$;
⑤ClO2很不穩定,步驟2所得溶液放置時間太長,ClO2分解相當于與碘反應,導致測定結果偏高,故答案為:偏高.
點評 本題考查實驗方案的設計,同時考查學生分析問題、解決問題的能力,把握習題中的信息及知識遷移應用為解答的關鍵,側重學生綜合應用能力及信息抽取和分析能力的考查,題目難度中等.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:解答題
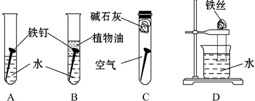 某研究性學習小組對鐵生銹進行研究.
某研究性學習小組對鐵生銹進行研究.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
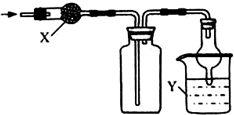
| 選項 | X | 收集氣體 | Y |
| A | 堿石灰 | 氯化氫 | 水 |
| B | 堿石灰 | 氨氣 | 水 |
| C | 無水氯化鈣 | 二氧化硫 | 氫氧化鈉 |
| D | 無水氯化鈣 | 一氧化氮 | 氫氧化鈉 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 陰極發生的電極反應為:2H++2e-=H2↑ | |
| B. | 在陽極室,通電后溶液逐漸由橙色變為黃色,是因為陽極區H+濃度增大,使平衡2CrO42-+2H+?Cr2O72-+H2O向右移動 | |
| C. | 該制備過程總反應的化學方程式為:4K2CrO4+4H2O$\frac{\underline{\;通電\;}}{\;}$2K2Cr2O7+4KOH+2H2↑+O2↑ | |
| D. | 測定陽極液中K和Cr的含量,若K與Cr的物質的量之比為d,則鉻酸鉀的轉化率為2-d |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
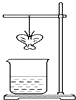 某同學用濾紙折成一個紙蝴蝶并噴灑一種溶液(保持濕潤),掛在鐵架臺上.另取一只盛某種溶液的燒杯,放在紙蝴蝶的下方(如圖).過一會,發現紙蝴蝶變為紅色.如表的組合中,能夠實現上述變化的是( )
某同學用濾紙折成一個紙蝴蝶并噴灑一種溶液(保持濕潤),掛在鐵架臺上.另取一只盛某種溶液的燒杯,放在紙蝴蝶的下方(如圖).過一會,發現紙蝴蝶變為紅色.如表的組合中,能夠實現上述變化的是( )| A | B | C | D | |
| 紙蝴蝶上的噴灑液 | 酚酞 | 酚酞 | 石蕊 | 石蕊 |
| 小燒杯中的溶液 | 濃氨水 | 濃NaOH | 濃鹽酸 | 濃硫酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
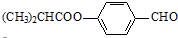 .合成M的一種途徑如下
.合成M的一種途徑如下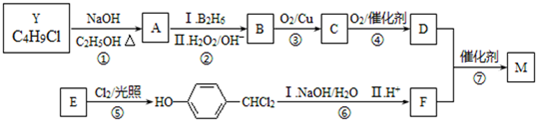
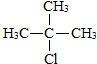 .
.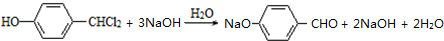 .
. .
.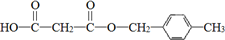 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. |  用裝置制取氯氣 | |
| B. | 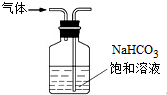 用裝置除去氯氣中混有的少量氯化氫 | |
| C. | 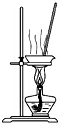 用裝置蒸干氯化錳溶液制MnCl2•4H2O | |
| D. | 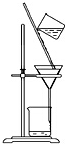 用裝置分離二氧化錳和氯化錳溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1 | |
| B. | 2H2(g)+O2(g)═2H2O(l)△H=+285.8 kJ•mol-1 | |
| C. | H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8 kJ•mol-1 | |
| D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-285.8 kJ•mol-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com