
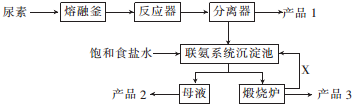
分析 尿素的熔點是132.7℃,常壓下超過160℃即可分解,三聚氰胺的熔點是354℃,加熱易升華,微溶于水,尿素在一定條件下分解生成三聚氰胺和氨氣、二氧化碳,飽和食鹽水加入聯氨系統沉淀池,所以產品1為三聚氰胺;從聯氨系統沉淀池中得到的母液中含有氯化銨,得到的沉淀是碳酸氫鈉,煅燒碳酸氫鈉得到二氧化碳,所以產品2是NH4Cl、產品3是Na2CO3、X是CO2,
(1)根據原子守恒配平方程式;在實驗室使尿素熔化的容器的名稱是坩堝;
(2)產品2是銨鹽,X是二氧化碳;
(3)聯氨系統沉淀池中發生反應生成氯化銨和碳酸氫鈉;
(4)要從母液中析出更多的碳酸氫鈉,根據反應CO2+NH3+NaCl+H2O→NH4Cl+NaHCO3,可以增大反應物濃度.
解答 解:尿素的熔點是132.7℃,常壓下超過160℃即可分解,三聚氰胺的熔點是354℃,加熱易升華,微溶于水,尿素在一定條件下分解生成三聚氰胺和氨氣、二氧化碳,飽和食鹽水加入聯氨系統沉淀池,所以產品1為三聚氰胺;從聯氨系統沉淀池中得到的母液中含有氯化銨,得到的沉淀是碳酸氫鈉,煅燒碳酸氫鈉得到二氧化碳,所以產品2是NH4Cl、產品3是Na2CO3、X是CO2,
(1)根據原子守恒配平方程式為6CO(NH2)2$\stackrel{一定條件}{→}$ C3N6H6+6NH3↑+3CO2↑,在實驗室使尿素熔化的容器的名稱是坩堝,故答案為:6;1;6;3;坩堝;
(2)通過以上分析知,產品2是NH4Cl,X是CO2,故答案為:NH4Cl;CO2;
(3)聯氨系統沉淀池中發生反應生成氯化銨和碳酸氫鈉,反應方程式為CO2+NH3+NaCl+H2O=NH4Cl+NaHCO3,故答案為:CO2+NH3+NaCl+H2O=NH4Cl+NaHCO3;
(4)要從母液中析出更多的碳酸氫鈉,根據反應CO2+NH3+NaCl+H2O→NH4Cl+NaHCO3,可以增大反應物濃度,所以可以向溶液中加入氯化鈉或者通入二氧化碳氣體,
故選AC.
點評 本題考查物質制備,為高頻考點,明確流程圖中發生的反應及實驗基本操作方法是解本題關鍵,熟悉氨堿法制備原理,題目難度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 操作 | 現象 |
| 取4g漂粉精固體,加入100mL水 | 部分固體溶解,溶液略有顏色 |
| 過濾,測漂粉精溶液的pH | pH試紙先變藍(約為12),后褪色 |
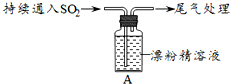 | i.液面上方出現白霧; ⅱ.稍后,出現渾濁,溶液變為黃綠色; ⅲ.稍后,產生大量白色沉淀,黃綠色褪去 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2種 | B. | 3種 | C. | 4種 | D. | 5種 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 元素 | 結構特點及元素、單質、化合物的性質 |
| X | 氣態氫化物與最高價氧化物對應水化物可以化合成鹽 |
| Y | 原子中s電子數與p電子數相同,且p電子的能量最高 |
| Z | 單質在空氣中燃燒產生黃色火焰,生成黃色粉末 |
| W | 最外層電子排布(n+1)sn(n+1)pn-1 |
| T | 單質升華可以產生紫色的煙 |
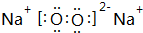 ;已知w 的氯化物在177.8°C時會發生升華現象,由此可以判斷它的晶體類型為分子晶體.
;已知w 的氯化物在177.8°C時會發生升華現象,由此可以判斷它的晶體類型為分子晶體.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金屬鋁投入到氫氧化鈉溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 三氯化鐵溶液中加入鐵粉 Fe3++Fe═2Fe2+ | |
| D. | 二氧化碳通入碳酸鈉溶液中:CO2+CO32-+H2O═2HCO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
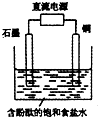
| A. | 銅電極上發生還原反應 | B. | 石墨電極附近溶液呈紅色 | ||
| C. | 溶液中的Na+向石墨電極移動 | D. | 銅電極附近觀察到黃綠色氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 弱電解質一定是共價化合物 | |
| B. | 氨氣溶于水,當c(OH-)=c(NH4+)時,表明NH3•H2O電離處于平衡狀態 | |
| C. | 強電解質溶液中不存在溶質分子,弱電解質溶液中存在溶質分子 | |
| D. | 由0.1 mol•L-1一元堿BOH的pH=10,可知溶液中存在BOH═B++OH- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com