
| A. | 最終三支試管的顏色各不相同 | |
| B. | A試管中Fe(OH)3含量最高 | |
| C. | 直接加熱蒸發(fā)Fe2(SO4)3溶液可得到Fe2(SO4)3晶體 | |
| D. | B試管中Fe2(SO4)3不能發(fā)生水解 |
分析 硫酸鐵溶液中鐵離子水解,溶液呈酸性,水解過程為吸熱反應,反應的離子方程式為Fe3++3H2O?Fe(OH)3+3H+,A試管加熱促進水解正向進行生成氫氧化鐵膠體,顏色變深,B中加入3滴6 mol/L H2SO4,氫離子濃度增加,水解平衡逆向進行鐵離子濃度增大.
解答 解:硫酸鐵溶液中鐵離子水解,溶液呈酸性,水解過程為吸熱反應,反應的離子方程式為Fe3++3H2O?Fe(OH)3+3H+,A試管加熱促進水解正向進行生成氫氧化鐵膠體,顏色變深,B中加入3滴6 mol/L H2SO4,氫離子濃度增加,水解平衡逆向進行鐵離子濃度增大;
A、上述分析可知,A中顏色加深,B中溶液顏色略微變深,最終三支試管的顏色各不相同,故A正確;
B、平衡移動方向分析可知,A中氫氧化鐵含量最高,故B正確;
C、直接加熱蒸發(fā)Fe2(SO4)3溶液,水解生成氫氧化鐵和硫酸,硫酸是難揮發(fā)性酸,加熱蒸發(fā)過程中是蒸發(fā)水,可得到Fe2(SO4)3晶體,故C錯誤;
D、B中是一致了水解平衡,不能抵消鐵離子的水解,故D正確;
故選C.
點評 本題考查了鹽類水解的分析應用,注意影響平衡的因素分析判斷,微粒濃度變化和溶液顏色變化的理解應用,掌握基礎是關鍵,題目難度中等.


 全能測控期末小狀元系列答案
全能測控期末小狀元系列答案科目:高中化學 來源: 題型:解答題
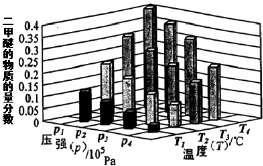
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
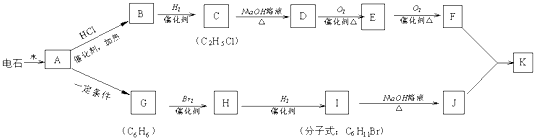
 ;
;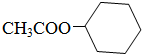 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
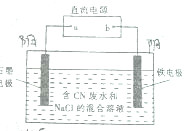 工業(yè)上,在強堿性條件下用電解法除去廢水中的CN-,裝制如圖所示,依次發(fā)生的反應有:
工業(yè)上,在強堿性條件下用電解法除去廢水中的CN-,裝制如圖所示,依次發(fā)生的反應有:| A. | a是電源的正極 | |
| B. | 鐵電極上發(fā)生的電極反應式為2H++2e-═H2↑ | |
| C. | 為了使電解池連續(xù)工作,需要不斷補充NaOH | |
| D. | 除去1mol CN-,電解過程中共產生標準狀況下11.2L氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 原子半徑大小順序:r(W)>r(Z)>r(Y)>r(X) | |
| B. | Y分別與Z、W形成的化合物中化學鍵類型相同 | |
| C. | X的最高價氧化物對應水化物的酸性比W的強 | |
| D. | Y的氣態(tài)簡單氫化物的熱穩(wěn)定性比W的強 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 描述 | 解釋或結論 |
| A | 向某溶液中加入BaCl2溶液生成白色沉淀,繼續(xù)加稀硝酸沉淀不消失 | 溶液中含SO42- |
| B | Cl2+H2O=HClO+HCl | Cl2僅為還原劑,HCl為氧化產物 |
| C | PH=1的溶液中Fe2+、Al3+、SO42-、MnO4-不能大量共存 | 5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O |
| D | SO2使酸性高錳酸鉀溶液和品紅試液褪色 | SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 目前,全世界鎳的消費量僅次于銅、鋁、鉛、鋅,居有色金屬第五位.鎳行業(yè)發(fā)展蘊藏著巨大潛力.
目前,全世界鎳的消費量僅次于銅、鋁、鉛、鋅,居有色金屬第五位.鎳行業(yè)發(fā)展蘊藏著巨大潛力. 、④HCHO等,其中分子屬于平面結構的有①②③④(填物質序號),預測HCHO分子的立體結構為平面三角形.
、④HCHO等,其中分子屬于平面結構的有①②③④(填物質序號),預測HCHO分子的立體結構為平面三角形. ,晶胞中心有一個鎳原子,其他鎳原子都在晶胞面上,鑭原子都在晶胞頂點上.該晶體的化學式為Ni5La或LaNi5.
,晶胞中心有一個鎳原子,其他鎳原子都在晶胞面上,鑭原子都在晶胞頂點上.該晶體的化學式為Ni5La或LaNi5.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 已知A、B、C、D、E、F、G、H八種元素都是周期表中前四周期的元素,它們的核電荷數依次增大,A是原子半徑最小是主族元素,B有三種不同的能級且每種能級上所含電子數相同,C的單質性質穩(wěn)定且一種氫化物極易溶于水,D能形成兩種互為同素異形體的氣態(tài)單質,A、D、E的核內質子數之和與F的核內質子數相同,F的基態(tài)原子中有4個未成對電子,G比F原子多一個核內質子,上述H元素的+1價陽離子的K、L、M能層為全充滿結構.
已知A、B、C、D、E、F、G、H八種元素都是周期表中前四周期的元素,它們的核電荷數依次增大,A是原子半徑最小是主族元素,B有三種不同的能級且每種能級上所含電子數相同,C的單質性質穩(wěn)定且一種氫化物極易溶于水,D能形成兩種互為同素異形體的氣態(tài)單質,A、D、E的核內質子數之和與F的核內質子數相同,F的基態(tài)原子中有4個未成對電子,G比F原子多一個核內質子,上述H元素的+1價陽離子的K、L、M能層為全充滿結構.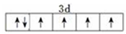 ;在這兩種離子之間Fe3+更穩(wěn)定(填化學式);從微觀結構角度解釋該離子更穩(wěn)定的原因:Fe3+離子的3d軌道為半滿穩(wěn)定狀態(tài).
;在這兩種離子之間Fe3+更穩(wěn)定(填化學式);從微觀結構角度解釋該離子更穩(wěn)定的原因:Fe3+離子的3d軌道為半滿穩(wěn)定狀態(tài).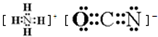 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com