
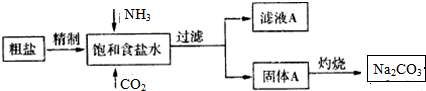
分析 (1)據根據SO42-、Ca 2+、Mg2+等易轉化為沉淀而被除去,以及根據不能產生新雜質的要求排序,前面加入的過量溶液應用后加入的溶液除去,最后加入適量的溶液;NH3易溶于水,有利于吸收溶解度不大的CO2;
(2)根據固體在坩堝加熱分解;
根據NH4+的檢驗方法:取少量濾液A于試管中,加入足量NaOH溶液并加熱,產生能使濕潤的紅色石蕊試紙變藍色的氣體,證明A中含有NH4+;NH4+和HCO3-都能與氫氧根離子反應;
(3)灼燒是將碳酸氫鈉分解成碳酸鈉;根據碳酸氫鈉受熱分解前后的固體質量變化可求得碳酸氫鈉的質量,進而計算純堿中碳酸氫鈉的質量分數.
解答 解:(1)①SO42-、Ca2+、Mg2+等分別與Ba(OH)2溶液、Na2CO3溶液、Ba(OH)2溶液反應生成沉淀,可再通過過濾除去,Na2CO3溶液能除去過量的Ba(OH)2溶液,鹽酸能除去過量的Na2CO3溶液和NaOH溶液,所以應先加Ba(OH)2溶液再加Na2CO3溶液,過濾,最后加入鹽酸,
故答案為:c;d;e;
②NH3易溶于水,有利于吸收溶解度不大的CO2,所以向飽和食鹽水中先通入NH3,后通人CO2,
故答案為:NH3易溶于水,有利于吸收溶解度不大的CO2;
(2)灼燒固體碳酸氫鈉制Na2CO3,在坩堝加熱分解,取少量濾液A于試管中,加入足量NaOH溶液并加熱,產生能使濕潤的紅色石蕊試紙變藍色的氣體,證明A中含有NH4+,NH4+和HCO3-都能與氫氧化鈉反應:NH4++HCO3-+2OH-=NH3•H2O+CO32-+H2O;
故答案為:a;取少量濾液A于試管中,加入足量NaOH溶液并加熱,產生能使濕潤的紅色石蕊試紙變藍色的氣體,證明A中含有NH4+;NH4++HCO3-+2OH-=NH3•H2O+CO32-+H2O;
(3)灼燒是將碳酸氫鈉分解成碳酸鈉,反應的方程式為2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+Na2CO3+H2O,加熱前固體質量為a g,充分加熱后質量變為b g,固體的質量差為(a-b)g,
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+Na2CO3+H2O△m
2×84 106 62
m (a-b)g
m=$\frac{84(a-b)}{31}$g,
所以純堿中碳酸氫鈉的質量分數ω(NaHCO3)=$\frac{\frac{84(a-b)}{31}}{a}$=$\frac{84(a-b)}{31a}$,
故答案為:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+Na2CO3+H2O;$\frac{84(a-b)}{31a}$.
點評 本題以制堿原理制取Na2CO3,涉及到物質的除雜和提純,常見的實驗操作,物質的制備等,難度中等,培養了學生運用知識的能力.


科目:高中化學 來源: 題型:解答題

| 密度(g/cm3) | 熔點(℃) | 沸點(℃) | 溶解性 | |
| 環己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 環己烯 | 0.81 | -103 | 83 | 難溶于水 |
 、SO2、CO2及水蒸氣,混合氣體通過試劑的順序是
、SO2、CO2及水蒸氣,混合氣體通過試劑的順序是
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


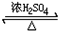 CH3COOCH2CH3+H2O,用飽和的碳酸鈉溶液(填藥品名稱)收集粗產品,用分液(填操作名稱)的方法把粗產品分離.
CH3COOCH2CH3+H2O,用飽和的碳酸鈉溶液(填藥品名稱)收集粗產品,用分液(填操作名稱)的方法把粗產品分離.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 如圖是甲、乙兩種物質的溶解度曲線.在t2℃時向盛有100g水的燒杯中先后加入wg甲和wg乙(兩種物質溶解時互不影響),充分攪拌.將混合物的溫度降低到t1℃.下列說法正確的是( )
如圖是甲、乙兩種物質的溶解度曲線.在t2℃時向盛有100g水的燒杯中先后加入wg甲和wg乙(兩種物質溶解時互不影響),充分攪拌.將混合物的溫度降低到t1℃.下列說法正確的是( )| A. | 甲物質的溶解度隨溫度升高而減小 | |
| B. | 溫度降低到t1℃時,得到甲、乙的飽和溶液 | |
| C. | 溫度降低到t1℃時,甲、乙的溶質質量分數相等,得到甲、乙的不飽和溶液 | |
| D. | t2℃時,甲物質的溶液為飽和溶液,乙物質的溶液為不飽和溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲苯能使酸性高錳酸鉀溶液褪色 | |
| B. | 甲苯與濃硫酸和濃硝酸混酸反應生成2,4,6-三硝基甲苯 | |
| C. | 1mol甲苯能與3mol氫氣發生加成反應 | |
| D. | 甲苯可以燃燒并產生濃烈的黑煙 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| ① | 氯化鐵溶液加熱蒸干最終得不到氯化鐵固體 | |
| ② | 鍍錫的鐵制品,鍍層部分受損后,露出的鐵表面更易被腐蝕 | |
| ③ | 電解精煉銅時,每轉移2mol電子陽極上溶解的銅原子數為NA | |
| ④ | 在lL0.1mol.L-1碳酸鈉溶液中,陰離子總數大于0.1NA |
| A. | ① | B. | ② | C. | ③ | D. | ④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{pq}{mt}$mol/(L.S) | B. | $\frac{mt}{pq}$mol/(L.S) | C. | $\frac{mp}{qt}$mol/(L.S) | D. | $\frac{tp}{mq}$mol/(L.S) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com