
| A. | 加催化劑,v正、v逆 都發生變化,且變化的倍數相等 | |
| B. | 加壓,v正、v逆 都增大,且v正 增大的倍數大于V逆增大的倍數 | |
| C. | 增大氮氣的濃度,N2的平衡轉化率減小,H2的平衡轉化率增大 | |
| D. | 降溫,v正、v逆 都減小,且v正 減小的倍數大于v逆減小的倍數 |
分析 該反應是一個反應前后氣體體積減小的、放熱反應,根據溫度、壓強、催化劑對反應速率和化學平衡的影響來分析解答.
解答 解:A.催化劑能同等程度的改變正逆反應速率,故A正確;
B.增大壓強,正逆反應速率都增大,但v正增大的倍數大于v逆增大的倍數,則平衡向正反應方向移動,故B正確;
C.增加一種反應物的濃度本身轉化率減小,另一種物質的轉化率變大,所以增大氮氣的濃度,N2的平衡轉化率減小,H2的平衡轉化率增大,故C正確;
D.降低溫度,正逆反應速率都減小,但正反應速率減小的倍數小于v逆減小的倍數,則平衡向正反應方向移動,故D錯誤;
故選D.
點評 本題考查了外界條件對化學反應速率和化學平衡的影響,易錯選項是C,增加一種反應物的濃度本身轉化率減小,另一種物質的轉化率變大,為易錯點.


科目:高中化學 來源: 題型:解答題
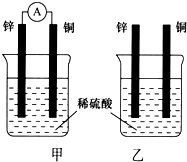 分別按下圖甲、乙所示裝置進行實驗,圖中兩個燒杯里的溶液為同濃度的稀硫酸,甲中A為電流表.請回答下列問題:
分別按下圖甲、乙所示裝置進行實驗,圖中兩個燒杯里的溶液為同濃度的稀硫酸,甲中A為電流表.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
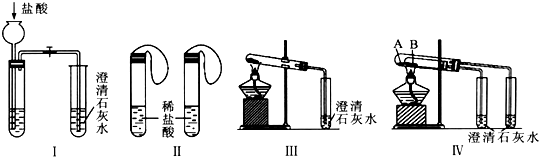
| 實驗方案 | 預測現象 | 預測依據 |
| 操作1:向2 mL Na2CO3溶液中滴加1 mL 0.5 mol•L-1 CaCl2溶液 | 有白色沉淀 | Na2CO3溶液中的CO32-濃度較大,能與CaCl2發生反應Ca2++CO32-=CaCO3↓(寫離子方程式) |
| 操作2:向2 mL NaHCO3溶液中滴加1 mL 0.5 mol•L-1 CaCl2溶液 | 無白色沉淀 | NaHCO3溶液中的CO32-濃度很小,不能與CaCl2反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{a}{b}$ | B. | $\frac{a}{2b}$ | C. | $\frac{a}{a+2b}$ | D. | $\frac{b}{a}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 苯氧乙酸甲酯的分子式為C9H10O3 | |
| B. | 苯氧乙酸與鄰羥基苯乙酸不互為同分異構體 | |
| C. | 苯酚和鄰羥基苯乙酸可用FeCl3溶液檢驗 | |
| D. | ClCH2COOH與足量燒堿溶液共熱所得有機物為HOCH2COOH |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
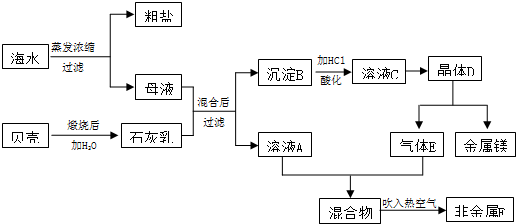
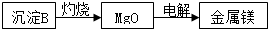
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 每摩爾花生四烯酸最多可與4 mol溴發生加成反應 | |
| B. | 它可以使酸性高錳酸鉀溶液褪色 | |
| C. | 它可與乙醇發生酯化反應 | |
| D. | 它是食醋的主要成分 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
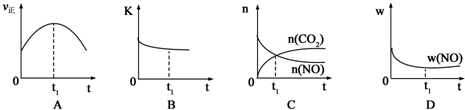
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com