
 .
.分析 有A、B、C、D、E五種短周期元素,它們的核電荷數按C、A、B、D、E的順序增大.E的M層電子數是K層電子數的2倍,則M層電子數為4,故E為Si;氣態物質EB4中B表現-1價,結合原子序數可知,B為F元素;C、D均能與A按原子個數比為1:1和2:1形成化合物,考慮是H、Na與氧元素形成的化合物,且CB可與EA2反應生成C2A與氣態物質EB4,應是HF與二氧化硅反應生成SiF4與水,故C為H元素、A為O元素、D為Na,據此解答.
解答 解:有A、B、C、D、E五種短周期元素,它們的核電荷數按C、A、B、D、E的順序增大.E的M層電子數是K層電子數的2倍,則M層電子數為4,故E為Si;氣態物質EB4中B表現-1價,結合原子序數可知,B為F元素;C、D均能與A按原子個數比為1:1和2:1形成化合物,考慮是H、Na與氧元素形成的化合物,且CB可與EA2反應生成C2A與氣態物質EB4,應是HF與二氧化硅反應生成SiF4與水,故C為H元素、A為O元素、D為Na.
(1)由上述分析可知,A、B、C、D、E五種元素的名稱為:氧、氟、氫、鈉、硅,
故答案為:氧、氟、氫、鈉、硅;
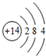
(2)E為Si,原子結構示意圖為 ,故答案為:
,故答案為: ;
;
(3)D2A2的化學式為Na2O2,故答案為:Na2O2;
(4)Na單質與銅鹽溶液反應的離子方程式:2Na+Cu2++2H2O=Cu(OH)2↓+H2↑+2Na+,
故答案為:2Na+Cu2++2H2O=Cu(OH)2↓+H2↑+2Na+.
點評 本題考查元素化合物推斷,推斷元素是解題關鍵,需要學生熟練掌握常見元素化合物的結構與性質,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 加催化劑,v正、v逆 都發生變化,且變化的倍數相等 | |
| B. | 加壓,v正、v逆 都增大,且v正 增大的倍數大于V逆增大的倍數 | |
| C. | 增大氮氣的濃度,N2的平衡轉化率減小,H2的平衡轉化率增大 | |
| D. | 降溫,v正、v逆 都減小,且v正 減小的倍數大于v逆減小的倍數 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
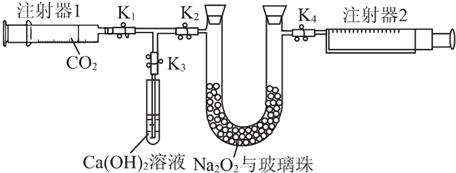
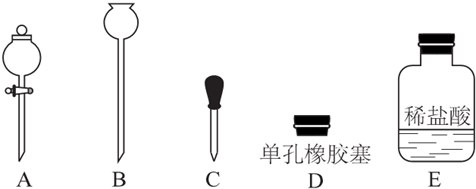
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
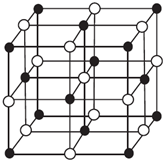 現有前四周期A、B、C、D、E、X六種元素,已知B、C、D、E、A五種非金屬元素原子半徑依次減小,其中B的s能級上電子總數等于p能級上電子總數的2倍.X原子的M能層上有4個未成對電子.請回答下列問題:
現有前四周期A、B、C、D、E、X六種元素,已知B、C、D、E、A五種非金屬元素原子半徑依次減小,其中B的s能級上電子總數等于p能級上電子總數的2倍.X原子的M能層上有4個未成對電子.請回答下列問題:| 離子晶體 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
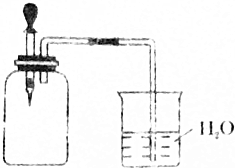 如圖所示,將1molCH4與1molCl2混合后充入集氣瓶內,置于光亮處,讓混合氣體緩慢地反應一段時間.
如圖所示,將1molCH4與1molCl2混合后充入集氣瓶內,置于光亮處,讓混合氣體緩慢地反應一段時間.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 離子半徑 | 熔點 | 酸性 |
| Cl- >Na+ | NaCl <C(金剛石) | H3PO4 <HClO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 檢驗溶液中是否含有Fe2+的方法是先滴加氯水,再滴加KSCN溶液 | |
| B. | 標準狀況下,將11.2LNO2和11.2LN2O4的混合,所得化合物所含分子數為NA | |
| C. | Na2CO3溶液加水稀釋后,恢復至原溫度,溶液的pH和Kw均減小 | |
| D. | 某電池的總反應為5MnO2+2Ag+2NaCl═Na2Mn5O10+2AgCl,每生成lmolNa2Mn5O10轉移電子數2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 滴加石蕊試液顯紅色的溶液:Fe3+、SO42-、C1-、SCN- | |
| B. | c(Al3+)=0.5mol•L的溶液中:Na+、K+、HCO3-、SO42- | |
| C. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=10 的溶液中:SO32-、NH4+、NO3-、K+ | |
| D. | 滴加甲基橙試液呈紅色的溶液:NH4+、Ba2+、Al3+、Cl- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com