
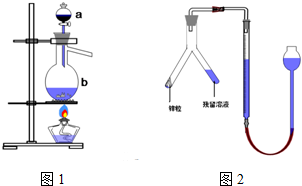
分析 (1)由儀器的結構可知,a為分液漏斗,b為蒸餾燒瓶;液體加熱需要防止暴沸;氯水具有漂白性,是由于HClO的強氧化性;
(2)儀器b中二氧化錳與濃鹽酸在加熱條件下反應生成氯化錳、氯氣與水;
(3)檢驗裝置氣密性后,向燒瓶中加入二氧化錳,再從分液漏斗中加入鹽酸,最后加熱制備氯氣;
(4)若殘留溶液轉移到鋅粒中,Y形管內壁會殘留溶液,HCl不能與Zn完全反應;
讀取體積時要滿足壓強回復到原壓強,而且眼的視線要與液體的凹液面相切;
甲同學的方案:二氧化錳與濃鹽酸反應生成氯化錳,也會與硝酸銀反應,實驗不可行.
解答 解:(1)由儀器的結構可知,a為分液漏斗,b為蒸餾燒瓶;b中加入碎瓷片的作用是:防止暴沸;氯水具有漂白性,是由于HClO的強氧化性,
故答案為:分液漏斗;蒸餾燒瓶;防止暴沸;HClO;
(2)儀器b中二氧化錳與濃鹽酸在加熱條件下反應生成氯化錳、氯氣與水,反應離子方程式為:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+Cl2↑,
故答案為:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+Cl2↑;
(3)檢驗裝置氣密性后,向燒瓶中加入二氧化錳,再從分液漏斗中加入鹽酸,最后加熱制備氯氣,
故答案為:A、C、D;
(4)若殘留溶液轉移到鋅粒中,Y形管內壁會殘留溶液,HCl不能與Zn完全反應,使測得的氣體的量不準確,測得的鹽酸的濃度不準,因此應將鋅粒轉移至殘留溶液中,
壓強對氣體的體積有影響,該反應是在加熱條件下進行的,溫度升高氣體壓強增大,如果不回復到原溫度,相當于將氣體壓縮了,使得測出的氣體的體積減小,故溫度要恢復到原溫度時,同時上下移動右端的漏斗,使兩端的液面的高度相同,視線要與液體的凹液面相切,讀取測量氣體的體積,
甲同學的方案中二氧化錳與濃鹽酸反應生成氯化錳,也會與硝酸銀反應,實驗不可行,乙同學方案可能,
故答案為:將鋅粒轉移至殘留溶液中;恢復至室溫;乙.
點評 本題考查氯氣的實驗室制備、物質含量測定實驗等,涉及化學儀器、對操作的分析評價、對實驗原理的分析評價等,是化學實驗綜合考查,難度中等.


科目:高中化學 來源: 題型:解答題
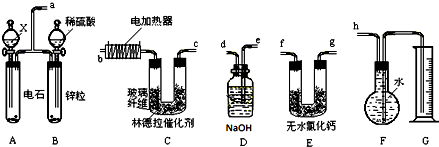
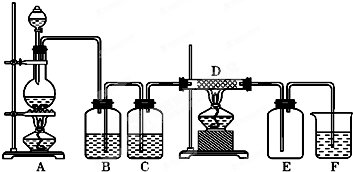 如圖所示,A是氯氣的發生裝置,B、C是凈化氣體的裝置,D中裝鐵絲網;反應后E的底部有棕色固體聚集;F是吸收多余氣體的裝置.
如圖所示,A是氯氣的發生裝置,B、C是凈化氣體的裝置,D中裝鐵絲網;反應后E的底部有棕色固體聚集;F是吸收多余氣體的裝置.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 如圖所示的裝置為鐵的吸氧腐蝕實驗.一段時間后,向插入鐵釘的玻璃筒內滴入K3[Fe(CN)6]溶液,可觀察到現象為鐵釘附近的溶液有藍色沉淀,該反應的離子方程式為Fe2++[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓; 向插入碳棒的玻璃筒內滴入酚酞溶液,可觀察到碳棒附近的溶液變紅,該電極反應為O2+4e-+2H2O=4OH.
如圖所示的裝置為鐵的吸氧腐蝕實驗.一段時間后,向插入鐵釘的玻璃筒內滴入K3[Fe(CN)6]溶液,可觀察到現象為鐵釘附近的溶液有藍色沉淀,該反應的離子方程式為Fe2++[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓; 向插入碳棒的玻璃筒內滴入酚酞溶液,可觀察到碳棒附近的溶液變紅,該電極反應為O2+4e-+2H2O=4OH.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
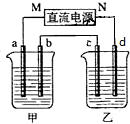 如圖所示裝置中,甲、乙兩個燒杯分別盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液,電極均為石墨電極.
如圖所示裝置中,甲、乙兩個燒杯分別盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液,電極均為石墨電極.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
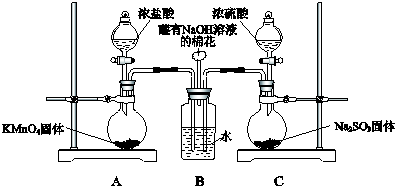
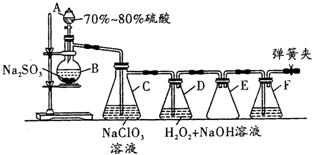 用二氧化氯(ClO2)可制備用途廣泛的亞氯酸鈉(NaClO2),實驗室可用如圖所示裝置(部分支持裝置省略)制備少量的亞氯酸鈉.
用二氧化氯(ClO2)可制備用途廣泛的亞氯酸鈉(NaClO2),實驗室可用如圖所示裝置(部分支持裝置省略)制備少量的亞氯酸鈉.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com