
 金屬鈦性能優越,被譽為繼Fe、Al后應用廣泛的“第三金屬”.
金屬鈦性能優越,被譽為繼Fe、Al后應用廣泛的“第三金屬”.分析 (1)Ti原子核外電子數為22,根據能量最低原理書寫核外電子排布式;
(2)同周期自左而右元素電負性增大;N原子中的2p軌道處于半充滿狀態,更穩定,第一電離能高于同周期相鄰元素的;
(3)SO42-中S原子孤電子對數=$\frac{6+2-2×4}{2}$=0,價層電子對數=4+0=4,雜化軌道數目為4,據此確定空間構型與雜化方式;原子數目相同、價電子總數相同的微粒互為等電子體;
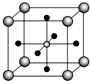
(4)CaTiO3的晶體結構中Ti4+位于立方體的頂點,由晶胞結構圖可知,體心為Ca2+,面心為O2-,該晶體中每個頂點Ti4+與面心的O2-相鄰,每個頂點為8個晶胞共用,每個面為2個晶胞共用;
(5)FexO晶體的晶胞結構為NaCl型,所以每個晶胞中含有4個O原子,有4個“FexO”,再根據m=ρV計算.
解答 解:(1)Ti原子核外電子數為22,根據能量最低原理,核外電子排布式為:1s22s22p63s23p63d24s2,
故答案為:1s22s22p63s23p63d24s2;
(2)同周期自左而右元素電負性增大,故電負性C>B,N原子中的2p軌道處于半充滿狀態,更穩定,第一電離能高于同周期相鄰元素的,故第一電離能N>O,
故答案為:>;>;N原子中的2p軌道處于半充滿狀態,更穩定;
(3)SO42-中S原子孤電子對數=$\frac{6+2-2×4}{2}$=0,價層電子對數=4+0=4,為正四面體結構,雜化軌道數目為4,S原子雜化方式為sp3;原子數目相同、價電子總數相同的微粒互為等電子體,SO42-的一種等電子體的化學式:ClO4-等,
故答案為:正四面體;sp3;ClO4-等;
(4)CaTiO3的晶體結構中Ti4+位于立方體的頂點,由晶胞結構圖可知,體心為Ca2+,面心為O2-,).該晶體中每個頂點Ti4+與面心的O2-相鄰,每個頂點為8個晶胞共用,每個面為2個晶胞共用,晶體中,Ti4+和周圍緊相鄰O2-數目為$\frac{3×8}{2}$=12,
故答案為:12;
(5)FexO晶體的晶胞結構為NaCl型,所以每個晶胞中含有4個O原子,有4個“FexO”,再根據m=ρV可知:4×$\frac{56x+16}{{N}_{A}}$g=5.71g•cm-3×(4.28×10-8 cm)3,解得:x=$\frac{{N}_{A}×5.71×(4.28×1{0}^{-8})^{3}}{4×56}$-$\frac{16}{56}$,
故答案為:$\frac{{N}_{A}×5.71×(4.28×1{0}^{-8})^{3}}{4×56}$-$\frac{16}{56}$.
點評 本題是對物質結構與性質的考查,涉及核外電子排布、電負性、電離能、空間構型與雜化方式判斷、等電子體、晶胞結構與計算,(5)中計算為易錯點、難點,注意識記中學常見晶胞結構,難度中等.


 導學全程練創優訓練系列答案
導學全程練創優訓練系列答案科目:高中化學 來源: 題型:選擇題
| A. | 空氣中:SO2、NO、N2、NH3 | |
| B. | 0.1mol/L的NaNO3溶液中:K+、I-、Cl-、SO42- | |
| C. | 鐵與稀硫酸反應后的溶液中:[Fe(CN)6]3-、NH4+、Cl-、NO3- | |
| D. | 與鋁反應生成大量氫氣的溶液中:Mg2+、K+、HCO3-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 改變條件,反應物的轉化率增大,平衡常數也一定增大 | |
| B. | 常溫下,V1L pH=12的NaOH溶液與V2L pH=2的HA溶液混合,若混合液顯中性,則V1≤V2 | |
| C. | 在0.1mol•L-1 NaHCO3溶液中,加入少量NaOH固體,Na+和CO32-的離子濃度均增大 | |
| D. | 反應2NO2(g)?N2O4(g)△H<O,升高溫度該反應平衡常數增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 任何酸與堿反應生成1 mol H2O的過程中,放出的熱量均相同 | |
| B. | 等量的硫蒸氣和硫固體分別完全燃燒,前者放出熱量多 | |
| C. | 光照時,H2(g)+Cl2(g)═2HCl(g)△H=aKJ/mol;若反應條件變為點燃,△H將減少 | |
| D. | 表示碳燃燒熱的熱化學方程式為:2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
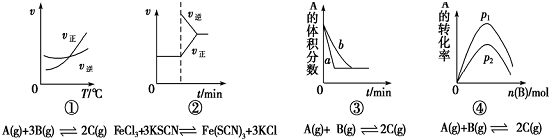
| A. | 圖①是其他條件一定時反應速率隨溫度變化的圖象,圖象表明,較低溫度下升溫平衡逆向移動,較高溫度下升溫平衡正向移 | |
| B. | 圖②是在平衡體系的溶液中加入少量KCl晶體后化學反應速率隨時間的變化 | |
| C. | 圖③可能是催化劑對化學平衡的影響,也可能是其它因素對化學平衡的影響 | |
| D. | 圖④是一定條件下,向含有一定量A的容器中逐漸加入B時的圖象,壓強p1>p2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 分子中含有4種官能團 | |
| B. | 分子式為C10H8O6 | |
| C. | 1mol分枝酸最多可與2mol乙醇發生酯化反應 | |
| D. | 可使溴的四氯化碳溶液、酸性高錳酸鉀溶液褪色,且原理相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 括號內為雜項 | 除雜試劑 | 除雜操作 | |
| A | Na2O2(Na2O) | O2 | 在純氧中加熱 |
| B | Na2CO3(NaHCO3) | CO2 | 通入過量的CO2 |
| C | FeCl(FeCl2) | Cl2 | 通入過量的Cl2 |
| D | FeSO4(CuSO4) | Fe | 加入過量的Fe粉,充分反應后過濾 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙烯使溴水褪色 | B. | 乙醇與濃硫酸共熱至170℃ | ||
| C. | 溴乙烷與NaOH水溶液共熱 | D. | 在液溴與苯的混合物中撒入鐵粉 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com