

 ,該分子的核磁共振氫譜有2種峰.
,該分子的核磁共振氫譜有2種峰.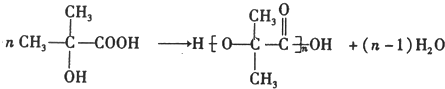 .F→G的反應:(CH3)2C(OH)-CHO+2Cu(OH)2$\stackrel{△}{→}$(CH3)2C(OH)-COOH+Cu2O↓+2H2O.
.F→G的反應:(CH3)2C(OH)-CHO+2Cu(OH)2$\stackrel{△}{→}$(CH3)2C(OH)-COOH+Cu2O↓+2H2O.分析 A是相對分子質量為92.5的飽和一氯代烴,分子中含有1個Cl原子,剩余烴基式量為92.5-35.5=57,利用商余法$\frac{57}{12}$=4…9,故烴基為-C4H9,A的分子式為C4H9Cl,分子中含有三個甲基,故A為C(CH3)3Cl,A在氫氧化鈉醇溶液中發生消去反應得到B為(CH3)2C=CH2,B發生加聚反應轉化為高分子化合物C為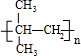 ,(CH3)2C=CH2與溴發生加成反應生成D為(CH3)2CBr-CH2Br,D在堿性條件下水解轉化為E為(CH3)2C(OH)-CH2OH,E發生氧化反應生成F為(CH3)2C(OH)-CHO,F氧化后酸得到G,則G為(CH3)2C(OH)-COOH,據此解答.
,(CH3)2C=CH2與溴發生加成反應生成D為(CH3)2CBr-CH2Br,D在堿性條件下水解轉化為E為(CH3)2C(OH)-CH2OH,E發生氧化反應生成F為(CH3)2C(OH)-CHO,F氧化后酸得到G,則G為(CH3)2C(OH)-COOH,據此解答.
解答 解:A是相對分子質量為92.5的飽和一氯代烴,分子中含有1個Cl原子,剩余烴基式量為92.5-35.5=57,利用商余法$\frac{57}{12}$=4…9,故烴基為-C4H9,A的分子式為C4H9Cl,分子中含有三個甲基,故A為C(CH3)3Cl,A在氫氧化鈉醇溶液中發生消去反應得到B為(CH3)2C=CH2,B發生加聚反應轉化為高分子化合物C為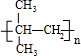 ,(CH3)2C=CH2與溴發生加成反應生成D為(CH3)2CBr-CH2Br,D在堿性條件下水解轉化為E為(CH3)2C(OH)-CH2OH,E發生氧化反應生成F為(CH3)2C(OH)-CHO,F氧化后酸得到G,則G為(CH3)2C(OH)-COOH,
,(CH3)2C=CH2與溴發生加成反應生成D為(CH3)2CBr-CH2Br,D在堿性條件下水解轉化為E為(CH3)2C(OH)-CH2OH,E發生氧化反應生成F為(CH3)2C(OH)-CHO,F氧化后酸得到G,則G為(CH3)2C(OH)-COOH,
(1)根據上面的分析可知,A的分子式為C4H9Cl,F為(CH3)2C(OH)-CHO,F中官能團的名稱為醛基、羥基,
故答案為:C4H9Cl;醛基、羥基;
(2)E為(CH3)2C(OH)-CH2OH,在濃硫酸加熱條件下,可以生成六元環狀化合物,其結構簡式為  ,該分子的核磁共振氫譜有2種峰,
,該分子的核磁共振氫譜有2種峰,
故答案為:(CH3)2C(OH)-CH2OH; ;2;
;2;
(3)G為(CH3)2C(OH)-COOH,G在一定條件下生成高分子化合物,反應的化學方程式為: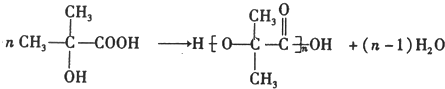 ,F→G的反應的化學方程式為(CH3)2C(OH)-CHO+2Cu(OH)2$\stackrel{△}{→}$(CH3)2C(OH)-COOH+Cu2O↓+2H2O,
,F→G的反應的化學方程式為(CH3)2C(OH)-CHO+2Cu(OH)2$\stackrel{△}{→}$(CH3)2C(OH)-COOH+Cu2O↓+2H2O,
故答案為: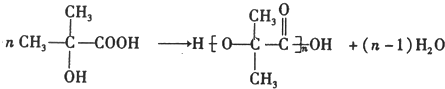 ;(CH3)2C(OH)-CHO+2Cu(OH)2$\stackrel{△}{→}$(CH3)2C(OH)-COOH+Cu2O↓+2H2O;
;(CH3)2C(OH)-CHO+2Cu(OH)2$\stackrel{△}{→}$(CH3)2C(OH)-COOH+Cu2O↓+2H2O;
(4)G為(CH3)2C(OH)-COOH,G的同分異構體于酯類,能發生銀鏡反應,為甲酸酯,能與金屬鈉反應放出氣體,還含有-OH,符合條件的同分異構體有:HOCH2CH2CH2OOCH,CH3CH(OH)CH2OOCH,CH3CH2CH(OH)OOCH,HCOOC(CH3)CH2OH,HCOOC(OH)(CH3)2,共五種,
故答案為:5.
點評 本題考查有機物的推斷,是對有機化學知識的綜合考查,推斷A的結構是解題的關鍵,能較好的考查學生的分析、思維能力,難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 若溫度不變,容器體積擴大一倍,此時A的濃度是原來的0.48倍,則a+b大于d | |
| B. | 若從正反應開始平衡時A、B的轉化率相等,則A、B的物質的量之比為a:b | |
| C. | 若平衡體系中氣體M mol,再充入bmolB,達到平衡氣體量為(M+b)mol,則a+b=c+d | |
| D. | 若a+b=d,則當容器內溫度上升時,平衡向左移動,容器中氣體的壓強不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
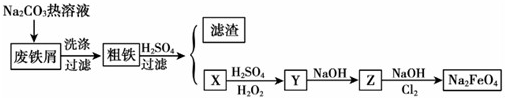
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 圖中所有的反應均為氧化還原反應 | |
| B. | 反應①②均為離子反應 | |
| C. | 反應②③都能產生氫氣,且產生等量氫氣消耗Al的質量和轉移電子數分別相等 | |
| D. | 反應①②⑦中鋁均作還原劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 主要原料:碳酸鈣 食用方法:每日一次,每次一片,嚼食. |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 如表為元素周期表的一部分,請參照元素①~⑧在表中的位置,回答下列問題:
如表為元素周期表的一部分,請參照元素①~⑧在表中的位置,回答下列問題: .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com