
| A. | 加入Al能放出H2的溶液中:ClO-、HCO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$、NH${\;}_{4}^{+}$ | |
| B. | pH=2的溶液中:Fe2+、Na+、Mg2+、NO${\;}_{3}^{-}$ | |
| C. | 能使KSCN溶液變紅的溶液中:Na+、I-、NO${\;}_{3}^{-}$、HCO${\;}_{3}^{-}$ | |
| D. | 由水電離出的c(OH-)=1.0×10-13mol•L-1的溶液中:Na+、Ba2+、Cl-、Br- |
分析 A.加入Al能放出H2的溶液可能呈酸性或堿性;
B.pH=2的溶液呈酸性;
C.能使KSCN溶液變紅的溶液含有Fe3+;
D.由水電離出的c(OH-)=1.0×10-13mol•L-1的溶液可能呈酸性或堿性.
解答 解:A.加入Al能放出H2的溶液可能呈酸性或堿性,無論呈酸性還是堿性,HCO3-都不能大量共存,故A錯誤;
B.pH=2的溶液呈酸性,酸性條件下Fe2+、NO3-發(fā)生氧化還原反應(yīng),故B錯誤;
C.能使KSCN溶液變紅的溶液含有Fe3+,與I-發(fā)生氧化還原反應(yīng),與HCO3-發(fā)生互促水解反應(yīng),故C錯誤;
D.由水電離出的c(OH-)=1.0×10-13mol•L-1的溶液可能呈酸性或堿性,離子之間不發(fā)生任何反應(yīng),可大量共存,故D正確.
故選D.
點評 本題考查離子的共存,為高考高頻考點,側(cè)重氧化還原反應(yīng)的離子共存問題的考查,注意信息的抽取和應(yīng)用,選項C為解答的難點,題目難度中等.


科目:高中化學(xué) 來源: 題型:選擇題
| A. | 分別加入碘水,觀察顏色反應(yīng) | |
| B. | 分別加稀硫酸煮沸,再加足量NaOH溶液調(diào)至堿性,加銀氨溶液加熱觀察有無銀鏡 | |
| C. | 分別加熱水溶解,觀察溶解性 | |
| D. | 放在嘴里咀嚼,有無甜味產(chǎn)生 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:選擇題
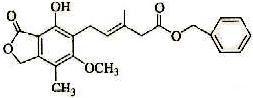
| A. | 一定條件下,既可以與Br2發(fā)生加成反應(yīng),又可以與Br2發(fā)生取代反應(yīng) | |
| B. | 1 mol該化合物最多可以與3 molNaOH反應(yīng) | |
| C. | 既可以催化加氫,又可以在稀硫酸存在下水解得2種有機物 | |
| D. | 可以與Na2CO3溶液反應(yīng)放出CO2氣體 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:解答題
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:解答題
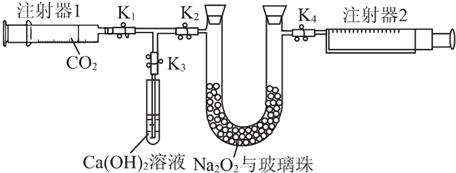
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:解答題
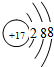 ;
;查看答案和解析>>
科目:高中化學(xué) 來源: 題型:解答題
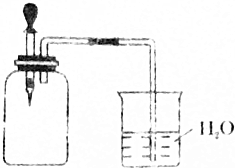 如圖所示,將1molCH4與1molCl2混合后充入集氣瓶內(nèi),置于光亮處,讓混合氣體緩慢地反應(yīng)一段時間.
如圖所示,將1molCH4與1molCl2混合后充入集氣瓶內(nèi),置于光亮處,讓混合氣體緩慢地反應(yīng)一段時間.查看答案和解析>>
科目:高中化學(xué) 來源: 題型:解答題
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:解答題

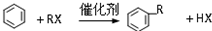 A具有和苯相似的性質(zhì).
A具有和苯相似的性質(zhì). 2HCHO+2H2O;
2HCHO+2H2O;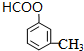 、
、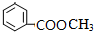 ;
;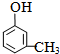 .
.查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com