
分析 ①Cu位于元素周期表第ⅠB族原子序數(shù)為29,根據(jù)Cu的電子排布式書寫Cu2+離子的電子排布式;
②Cu2O與Cu2S都為離子晶體,離子半徑越小,離子鍵越強,對應的熔點越高.
解答 解:①Cu(電子排布式為:[Ar]3d104s1)Cu2+的過程中,參與反應的電子是最外層的4s及3d上各一個電子,故Cu2+離子的電子排布式是為:[Ar]3d9或1s22s22p63s23p63d9,故答案為:[Ar]3d9或1s22s22p63s23p63d9;
②Cu2O與Cu2S都為離子晶體,離子半徑越小,離子鍵越強,對應的熔點越高,因氧離子半徑比硫離子半徑小,Cu2O比Cu2S的離子鍵強,所以Cu2O熔點高.
故答案為:高;氧離子半徑比硫離子半徑小,Cu2O比Cu2S的離子鍵強,所以Cu2O熔點高.
點評 本題考查常見元素核外電子排布、離子鍵以及晶格能等知識,為高頻考點,題目難度中等,學習中注意加強對核外電子排布的學習.


科目:高中化學 來源: 題型:解答題
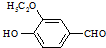 )是食品添加劑的增香原料,其香味比香草醛更加濃郁.
)是食品添加劑的增香原料,其香味比香草醛更加濃郁.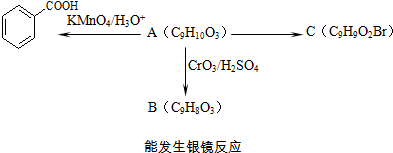
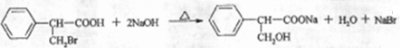
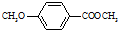 )是一種醫(yī)藥中間體.
)是一種醫(yī)藥中間體. )合成D.用反應流程圖表示如下,請將后面一步的反應條件寫在箭頭下方,試劑或原料寫在箭頭上方,中間產(chǎn)物填在圖中的方框內(nèi).
)合成D.用反應流程圖表示如下,請將后面一步的反應條件寫在箭頭下方,試劑或原料寫在箭頭上方,中間產(chǎn)物填在圖中的方框內(nèi).
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 燃煤時加入適量石灰石,可減少廢氣中SO2的含量 | |
| B. | 京津冀、長三角、珠三角霧霾的形成與煤的燃燒、化工廠大量排放含硫、含氮氧化物、顆粒物和汽車排放的尾氣等有關 | |
| C. | pH小于7.0的降雨通常稱為酸雨 | |
| D. | 使用潔凈能源、為汽車安裝尾氣轉化裝置、對硝酸廠排放的廢氣進行堿處理能有效控制氮氧化物對空氣的污染 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 構造原理 | B. | 泡利不相容原理 | C. | 洪特規(guī)則 | D. | 能量最低原理 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 濃硝酸應保存在棕色試劑瓶并置于陰涼處 | |
| B. | 氫氟酸不能裝在玻璃瓶,應裝在塑料瓶中 | |
| C. | NaOH溶液用帶磨口玻璃瓶塞的試劑瓶保存 | |
| D. | 常溫下濃硫酸和濃硝酸可以鐵制槽罐車運輸 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 小于0.9mol | B. | 等于0.9mol | ||
| C. | 在0.45mol與0.9mol之間 | D. | 大于0.9mol |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com