
| A. | 甲燒杯中放入鋅的質量比乙燒杯中放入鋅的質量大 | |
| B. | 甲燒杯中的酸過量 | |
| C. | 甲燒杯比乙燒杯反應快 | |
| D. | 反應開始后乙燒杯中的c(H+)始終比甲燒杯中的c(H+)小 |
分析 A.醋酸濃度大,等體積的兩種酸,醋酸的物質的量大于鹽酸,產生等量的氫氣,醋酸中鋅的量要少與鹽酸中鋅的量;
B.鹽酸的濃度小,生成等量的氫氣,鹽酸完全反應;
C.由于醋酸還能繼續電離而鹽酸不能,所以反應開始后,醋酸中的H+濃度大于鹽酸中的氫離子濃度;
D.反應開始后,醋酸持續電離.
解答 解:A.在體積和pH都相等的鹽酸和醋酸中,已提供的H+的濃度和其物質的量相等,但由于醋酸是弱酸,只有部分電離,鹽酸是強酸,已經完全電離,所以可提供的H+的物質的量顯然是醋酸大于鹽酸,與足量的鋅反應時,消耗鋅的質量是醋酸大于鹽酸,要使兩種酸中生成的氫氣的量相等,則在醋酸中加入的鋅粒質量應較小,鹽酸中加入的鋅粒質量較大,故A正確;
B.當加入的鋅粒質量不等而產生等量的氫氣時,說明參加反應的鋅粒相等,鹽酸中加入的鋅粒質量較大,鹽酸一定完全反應,乙燒杯中醋酸一定有剩余,故B錯誤;
C.由于醋酸還能繼續電離而鹽酸不能,所以反應開始后,醋酸中的H+濃度大于鹽酸中的氫離子濃度,乙比甲快,故C錯誤;
D.由于醋酸還能繼續電離而鹽酸不能,所以反應開始后,醋酸中的H+濃度大于鹽酸中的氫離子濃度,則反應開始后乙燒杯中的C(H+)始終比甲燒杯中的c(H+)大,故D錯誤;
故選A.
點評 本題考查了強弱酸與金屬反應的有關問題,明確弱電解質電離特點是解本題關鍵,結合轉移電子相等、氫離子與酸濃度的關系來分析解答,難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 1mol H2含有的分子數目為NA | |
| B. | 24g Mg變為Mg2+時失去的電子數目為NA | |
| C. | 1L 1mol•L-1CaCl2溶液中含有的Cl-離子數目為NA | |
| D. | 常溫常壓下,11.2LO2中含有的原子數目為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 滴有酚酞的碳酸氫鈉溶液顯紅色,微熱后紅色加深,是因為碳酸氫鈉分解生成了碳酸鈉 | |
| B. | 用潔凈的玻璃管向包有過氧化鈉的脫脂棉吹氣,脫脂棉燃燒,說明二氧化碳、水與過氧化鈉的反應是放熱反應 | |
| C. | 向溴水中滴入植物油,振蕩后油層顯無色,說明溴不溶于油脂 | |
| D. | 粗鋅與稀硫酸反應制氫氣比純鋅快,是因為粗鋅比純鋅還原性強 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
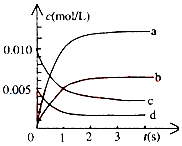 在2L密閉容器中,800℃時反應2NO(g)+O2(g)?2NO2(g)體系中,n(NO)隨時間的變化如表:
在2L密閉容器中,800℃時反應2NO(g)+O2(g)?2NO2(g)體系中,n(NO)隨時間的變化如表:| 時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
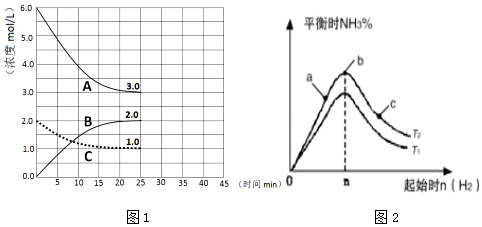
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
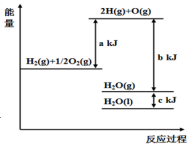
| A. | 1 mol H2(g)與$\frac{1}{2}$ mol O2(g)所具有的總能量比1 mol H2O(g)所具有的總能量高 | |
| B. | H2O(g)生成H2O(l)時,斷鍵吸收的能量小于成鍵放出的能量 | |
| C. | 2 mol H(g)與1 mol O(g)生成1 molH2O(g)所放出的熱量是b kJ | |
| D. | 液態水分解的熱化學方程式為:2H2O(l)═2H2(g)+O2(g)△H=2(b+c-a)kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
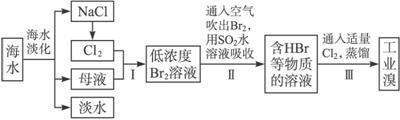
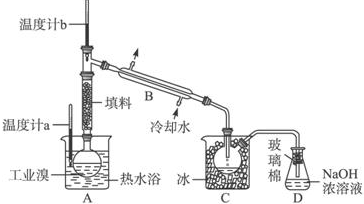
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

 .
. .
.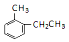 的名稱是2-甲基乙苯.
的名稱是2-甲基乙苯. +CH3COOH$?_{△}^{濃H_{2}SO_{4}}$
+CH3COOH$?_{△}^{濃H_{2}SO_{4}}$ +H2O.
+H2O. 的一種同分異構體的結構簡式
的一種同分異構體的結構簡式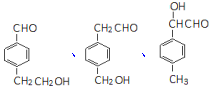 任一種.
任一種.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com