

| 相對分子質量 | 密度/(g•cm-3) | 沸點/℃ | 溶解性 | |
| 環己醇 | 100 | 0.961 8 | 161 | 微溶于水 |
| 環己烯 | 82 | 0.810 2 | 83 | 難溶于水 |

分析 (1)根據裝置圖可知裝置b的名稱;
(2)碎瓷片的存在可以防止在加熱過程中產生暴沸現象,補加碎瓷片時需要待已加熱的試液冷卻后再加入;
(3)加熱過程中,環己醇除可發生消去反應生成環己烯外,還可以發生取代反應生成二環己醚;
(4)由于分液漏斗有活塞開關,故使用前需要檢查是否漏液;分液過程中,由于環己烯的密度比水的密度小,故應該從分液漏斗的上口倒出;
(5)無水氯化鈣用于吸收產物中少量的水;
(6)觀察題目提供的實驗裝置圖知蒸餾過程中不可能用到吸濾瓶和球形冷凝器管;
(7)環己醇為0.2mol,根據反應方程式,理論上可以得到0.2mol環己烯,其質量為16.4g,根據產率=$\frac{實際產量}{理論產量}$×100%計算
解答 解:(1)依據裝置圖分析可知裝置b是蒸餾裝置中的冷凝器裝置,
故答案為:直形冷凝器;
(2)碎瓷片的存在可以防止在加熱過程中產生暴沸現象,補加碎瓷片時需要待已加熱的試液冷卻后再加入,故選B,
故答案為:防止暴沸;B;
(3)加熱過程中,環己醇除可發生消去反應生成環己烯外,還可以發生取代反應,分子間發生脫水反應生成二環己醚為 ,
,
故答案為: ;
;
(4)由于分液漏斗有活塞開關,故使用前需要檢查是否漏液;分液過程中,由于環己烯的密度比水的密度小,故應該從分液漏斗的上口倒出,
故答案為:檢漏;上口倒出;
(5)分離提純過程中加入無水氯化鈣的目的是利用無水氯化鈣吸收產物中少量的水,
故答案為:干燥;
(6)觀察題目提供的實驗裝置圖知蒸餾過程中不可能用到吸濾瓶和球形冷凝器管,
故選:CD;
(7)環己醇為0.2mol,理論上可以得到0.2mol環己烯,其質量為16.4g,所以產率=$\frac{10g}{16.4g}$×100%=61%,
故選C.
點評 本題考查了物質制備實驗方案設計,醇性質的分析應用,實驗現象和原理的分析判斷,掌握基礎是解題關鍵,題目難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:多選題
| A. | 被測樣品中含有加熱不揮發的雜質 | B. | 被測樣品中含有加熱易揮發的雜質 | ||
| C. | 實驗前被測樣品已有部分失水 | D. | 加熱前所用的坩堝未完全干燥 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 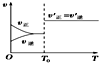 反應H2(g)+I2(g)?2HI(g)達到平衡后,升高溫度時反應速率隨時間的變化 | |
| B. | 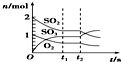 反應2SO2(g)+O2(g)?2SO3(g)達到平衡后,縮小容器容積時各成分的物質的量隨時間的變化 | |
| C. |  反應N2(g)+3H2(g)?2NH3(g)在恒溫條件下,反應速率與壓強的關系 | |
| D. |  反應CO2(g)+H2(g)?CO(g)+H2O(g)△H>0水蒸氣含量隨時間的變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ②⑤①③④ | B. | ①③⑤②④ | C. | ①②③④⑤ | D. | ②①③⑤④ |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
 如圖為實驗室制備乙烯的裝置圖,請回答:
如圖為實驗室制備乙烯的裝置圖,請回答:查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
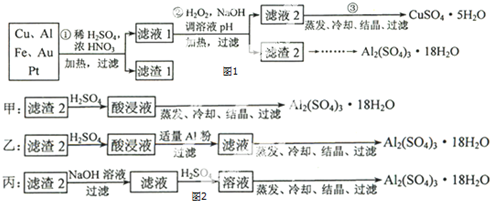
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
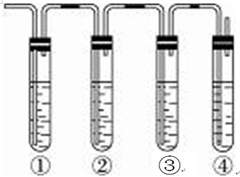 實驗室制取乙烯,常因溫度過高而使乙醇和濃H2SO4反應生成少量的SO2,有人設計下列實驗確認上述混合氣體中有乙烯和二氧化硫.A.品紅溶液 B.NaOH溶液 C.濃硫酸 D.高錳酸鉀酸性溶液.試完成下列問題:
實驗室制取乙烯,常因溫度過高而使乙醇和濃H2SO4反應生成少量的SO2,有人設計下列實驗確認上述混合氣體中有乙烯和二氧化硫.A.品紅溶液 B.NaOH溶液 C.濃硫酸 D.高錳酸鉀酸性溶液.試完成下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④⑤ | B. | ②⑤⑥⑧ | C. | ②③⑥⑧ | D. | ⑤⑥⑦ |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 第一電離能由大到小的順序為O>N>C | |
| B. | NO3-中N采用sp2雜化,故NO3-的空間構型為三角錐形 | |
| C. | 由于C22-和O22+為等電子體,所以可以判斷O22+的電子式為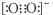 | |
| D. | 液態HF通常也可以寫成(HF)n的形式,是因為液態HF分子間存在氫鍵 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com