
| A. | ①④⑤ | B. | ②⑤⑥⑧ | C. | ②③⑥⑧ | D. | ⑤⑥⑦ |
分析 灼燒硫酸銅晶體制取無水硫酸銅所需用的儀器有灼燒藥品的儀器坩堝、夾取坩堝的儀器坩堝鉗,放置坩堝的三腳架、泥三角,攪拌藥品的玻璃棒、冷卻坩堝的儀器干燥器、加熱的儀器酒精燈,據此分析解答.
解答 解:灼燒硫酸銅晶體制取無水硫酸銅所需用的儀器有灼燒藥品的儀器坩堝、夾取坩堝的儀器坩堝鉗,放置坩堝的三腳架、泥三角,攪拌藥品的玻璃棒、冷卻坩堝的儀器干燥器、加熱的儀器酒精燈,所以需要的儀器有酒精燈、三腳架、泥三角、坩堝、坩堝鉗、玻璃棒、干燥器,
故選B.
點評 本題以結晶水測定,為高頻考點,明確儀器用途是解本題關鍵,側重考查學生對儀器用途的了解及實驗操作規范性,根據實驗目的及儀器“從下而上”選取儀器,注意:加熱坩堝應該放置在干燥器中干燥,而不是放置在空氣中干燥,為易錯點.


 一本好題口算題卡系列答案
一本好題口算題卡系列答案科目:高中化學 來源: 題型:解答題


查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 相對分子質量 | 密度/(g•cm-3) | 沸點/℃ | 溶解性 | |
| 環己醇 | 100 | 0.961 8 | 161 | 微溶于水 |
| 環己烯 | 82 | 0.810 2 | 83 | 難溶于水 |

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①和② | B. | ①和③ | C. | ②和③ | D. | ①②③ |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
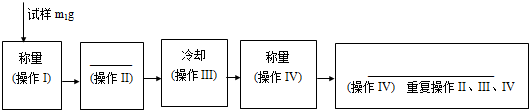
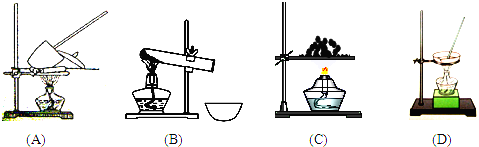
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
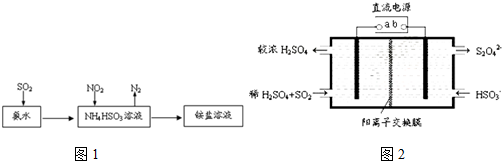
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
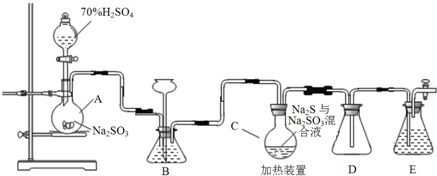
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 增大壓強,化學平衡不一定發生移動 | |
| B. | 通入與反應無關的氦氣,化學平衡不發生移動 | |
| C. | 增大X或Y的物質的量,化學平衡一定發生移動 | |
| D. | 其它條件不變,升高溫度,化學平衡一定發生移動 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com