


分析 (1)(2)檢驗二氧化硫可用品紅溶液,檢驗二氧化碳可以用澄清石灰水,檢驗水用無水硫酸銅,三者都有時,應先通過無水硫酸銅檢驗水蒸氣的存在,因為在驗證二氧化碳、二氧化硫的存在時都需通過溶液,可帶出水蒸氣;二氧化碳、二氧化硫都能使澄清的石灰水變渾濁,所以不能先通過澄清的石灰水來檢驗二氧化碳的存在,二氧化碳的檢驗應放在排除SO2的干擾后進行,所以應先無水硫酸銅檢驗水蒸氣的存在,通過品紅溶液褪色檢驗SO2的存在,再通過酸性高錳酸鉀溶液除去SO2,再通過品紅溶液不褪色確認SO2已除干凈,最后用澄清石灰水實驗檢驗二氧化碳;
(3)用澄清石灰水實驗檢驗二氧化碳;
(4)先通過無水硫酸銅檢驗水蒸氣的存在,因為在驗證二氧化碳、二氧化硫的存在時都需通過溶液,可帶出水蒸氣;
(5)乙烯在一定條件下發生的是聚合反應能制得聚乙烯;
(6)實驗室通常用無水乙醇和濃硫酸加熱到170℃制取乙烯,需要溫度計測定溶液溫度.
解答 解:(1)檢驗二氧化硫可用品紅溶液,檢驗二氧化碳可以用澄清石灰水,檢驗水用無水硫酸銅,三者都有時,應先檢驗水蒸氣的存在,因為在驗證二氧化碳、二氧化硫的存在時都需通過溶液,可帶出水蒸氣;二氧化碳、二氧化硫都能使澄清的石灰水變渾濁,所以不能先通過澄清的石灰水來檢驗二氧化碳的存在,二氧化碳的檢驗應放在排除SO2的干擾后進行,所以應先通過品紅溶液褪色檢驗SO2的存在,再通過酸性高錳酸鉀溶液除去SO2,再通過品紅溶液不褪色確認SO2已除干凈,最后用澄清石灰水實驗檢驗二氧化碳;
故答案為:④②①③;
(2)檢驗二氧化硫可用品紅溶液,二氧化碳、二氧化硫都能使澄清的石灰水變渾濁,二氧化碳的檢驗應放在排除SO2的干擾后進行,所以應先通過品紅溶液褪色檢驗SO2的存在,再通過酸性高錳酸鉀溶液除去SO2,接著通過品紅溶液不褪色確認SO2已除干凈;
故答案為:除去或吸收SO2;檢驗SO2是否除盡;
(3)用澄清石灰水實驗檢驗二氧化碳,若氣體通過裝置③中所盛溶液澄清石灰水時,產生白色沉淀,
故答案為:CO2;
(4)先通過無水硫酸銅檢驗水蒸氣的存在,因為在驗證二氧化碳、二氧化硫的存在時都需通過溶液,可帶出水蒸氣,影響水蒸氣的確定;
故答案為:無水硫酸銅;
(5)乙烯在一定條件下能制得聚乙烯,發生的是聚合反應,反應的化學方程式為: ,
,
故答案為: ;
;
(6)實驗室通常用無水乙醇和濃硫酸加熱到170℃制取乙烯,需要溫度計測定溶液溫度;
故答案為:發生裝置④中缺少溫度計.
點評 本題考查乙烯的化學性質、制備以及常見氣體的檢驗,題目難度中等,注意實驗原理及檢驗的先后順序.


科目:高中化學 來源: 題型:選擇題

| A. | 圖甲:進行中和熱的測定 | |
| B. | 圖乙:比較 HCl、H2CO3和 H2SiO3 的酸性強弱 | |
| C. | 圖丙:驗證 CuCl2對 H2O2 分解有催化作用 | |
| D. | 圖丁:驗證 2NO2(g)?N2O4(g)△H<0 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 被測樣品中含有加熱不揮發的雜質 | B. | 被測樣品中含有加熱易揮發的雜質 | ||
| C. | 實驗前被測樣品已有部分失水 | D. | 加熱前所用的坩堝未完全干燥 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
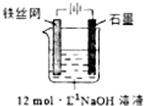 高鐵酸鉀(K2FeO4)是一種高效多功能水處理劑,具有極強的氧化性.
高鐵酸鉀(K2FeO4)是一種高效多功能水處理劑,具有極強的氧化性.| 干法 | Fe2O3、KNO3、KOH混合加熱共熔生成紫紅色高鐵酸鹽和KNO2等產物 |
| 濕法 | 強堿性介質中,Fe(NO3)3與NaClO反應生成紫紅色高鐵酸鹽溶液 |
| 電解法 | 制備中間產物Na2FeO4,再與KOH溶液反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
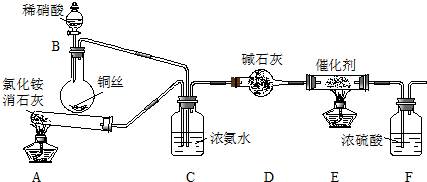
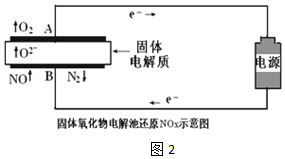
| 實驗序號 | B極氣體 | 電路中通過電子 | 消耗總電能 | 生成N2 |
| 實驗1 | NO | 1mol | a KJ | 0.25mol |
| 實驗2 | NO和空氣 (不考慮NO2) | 1mol | a KJ | 0.09mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
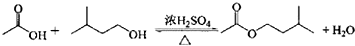
| 相對原子質量 | 密度/(g.cm-3) | 沸點/℃ | 水中溶解性 | |
| 異戊醇 | 88 | 0.813 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸異戊醇 | 130 | 0.8670 | 142 | 難溶 |
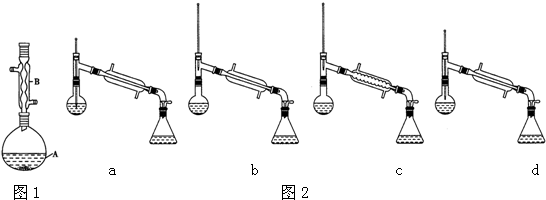
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 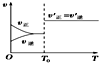 反應H2(g)+I2(g)?2HI(g)達到平衡后,升高溫度時反應速率隨時間的變化 | |
| B. | 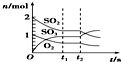 反應2SO2(g)+O2(g)?2SO3(g)達到平衡后,縮小容器容積時各成分的物質的量隨時間的變化 | |
| C. |  反應N2(g)+3H2(g)?2NH3(g)在恒溫條件下,反應速率與壓強的關系 | |
| D. |  反應CO2(g)+H2(g)?CO(g)+H2O(g)△H>0水蒸氣含量隨時間的變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ②⑤①③④ | B. | ①③⑤②④ | C. | ①②③④⑤ | D. | ②①③⑤④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④⑤ | B. | ②⑤⑥⑧ | C. | ②③⑥⑧ | D. | ⑤⑥⑦ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com