
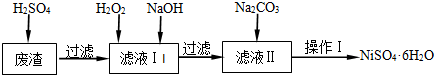
| Fe(OH)2 | Fe(OH)3 | Cr(OH)3 | Ni(OH)2 | |
| Ksp | 8.0×10-16 | 4.0×10-38 | 6.0×10-31 | 6.5×10-18 |
| 完全沉淀pH | ≥9.6 | ≥3.2 | ≥5.6 | ≥8.4 |


科目:高中化學 來源: 題型:
| A、將Al2O3溶于水 |
| B、將Al2O3先溶于鹽酸中,之后滴加氫氧化鈉溶液 |
| C、將Al2O3先溶于鹽酸中,之后滴加氨水 |
| D、將Al2O3先溶于NaOH溶液中,之后再滴加鹽酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:
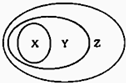 如圖用交叉分類法表示了一些物質或概念之間的從屬或包含關系,其中正確的是 ( )
如圖用交叉分類法表示了一些物質或概念之間的從屬或包含關系,其中正確的是 ( )| X | Y | Z | |
| A | 置換反應 | 氧化還原反應 | 離子反應 |
| B | 銅 | 單質 | 非電解質 |
| C | 石灰水 | 電解質 | 分散系 |
| D | 液氨 | 化合物 | 純凈物 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化學 來源: 題型:
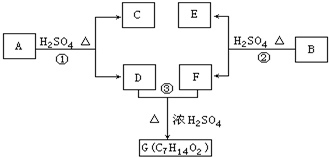 以下各種有機化合物之間有如圖的轉化關系:
以下各種有機化合物之間有如圖的轉化關系:查看答案和解析>>
科目:高中化學 來源: 題型:
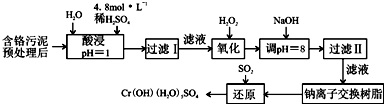
| 陽離子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| 開始沉淀時的pH | 1.9 | 7.0 | -- | -- | 4.7 | -- |
| 沉淀完全時的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9 (>9溶解) |
查看答案和解析>>
科目:高中化學 來源: 題型:
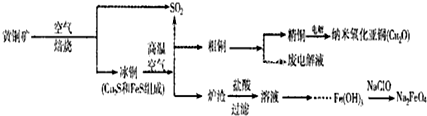
| ||
| ||
n(SO
| 91:9 | 1:1 | 1:91 | ||||
| PH(25℃) | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
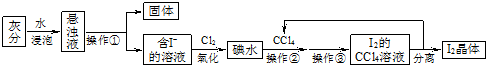
查看答案和解析>>
科目:高中化學 來源: 題型:
 有X、Y、Z三種短周期元素,原子半徑的大小關系為r(Y)>r(X)>r(Z),原子序數之和為16.X、Y、Z三種元素的常見單質在適當條件下可發生如下變化,其中B和C均為10電子分子.下列說法中不正確的是( )
有X、Y、Z三種短周期元素,原子半徑的大小關系為r(Y)>r(X)>r(Z),原子序數之和為16.X、Y、Z三種元素的常見單質在適當條件下可發生如下變化,其中B和C均為10電子分子.下列說法中不正確的是( )| A、X元素位于ⅥA |
| B、熱穩定性:B>C |
| C、C極易溶于B中,溶液呈堿性 |
| D、A和C不可能發生氧化還原反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、金屬鋁溶于氫氧化鈉溶液:Al+2OH-+2H2O=[Al(OH)4]-+H2↑ |
| B、過量鐵溶于稀硝酸:Fe+4H++NO3-═Fe3++NO↑+2H2O |
| C、用食醋除去暖水瓶中的水垢:2CH3COOH+CaCO3═Ca2++2CH3COO-+CO2↑+H2O |
| D、Ca(HCO3)2溶液中加入少量的NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com