
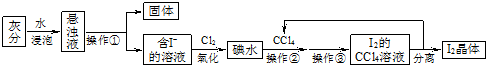


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
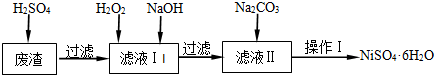
| Fe(OH)2 | Fe(OH)3 | Cr(OH)3 | Ni(OH)2 | |
| Ksp | 8.0×10-16 | 4.0×10-38 | 6.0×10-31 | 6.5×10-18 |
| 完全沉淀pH | ≥9.6 | ≥3.2 | ≥5.6 | ≥8.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:
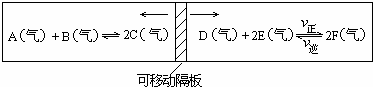
查看答案和解析>>
科目:高中化學 來源: 題型:
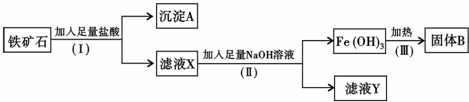
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 完全沉淀的pH | 5.2 | 3.2 | 9.0 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 3 |
| 4 |
查看答案和解析>>
科目:高中化學 來源: 題型:
A、 檢查裝置氣密性 |
B、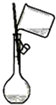 向容量瓶中轉(zhuǎn)移液體 |
C、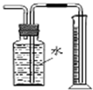 測量Cu與濃硝酸產(chǎn)生氣體體積 |
D、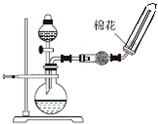 實驗室制取并收集NH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:
A、蒸發(fā)時,蒸發(fā)皿內(nèi)所盛液體不超過蒸發(fā)皿容積的
| ||
| B、蒸發(fā)結(jié)晶時,不能直接蒸干液體,最后少量液體用余熱蒸干 | ||
| C、用四氯化碳萃取碘水中的碘,分液時四氯化碳碘溶液從上口倒出 | ||
| D、蒸餾時,要在燒瓶中加入幾粒碎瓷片 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com